1968 - Il trattamento emodialitico dell’insufficienza renale cronica
Tratto dalla tesi di laurea:
"Il trattamento Emodialitico dell'insufficienza renale cronica"
di Giuliano Giachino
Università degli Studi di Torino
Facoltà di Medicina e Chirurgia
anno accademico 1967-68

Dalla sua introduzione nella pratica clinica sino a questi ultimi anni l’emodialisi extracorporea è stata considerata come un mezzo di trattamento quasi esclusivamente riservato all’insufficienza renale acuta. Lo stesso Kolff, il primo a compiere esperienze cliniche con una attrezzatura da lui ideata, negli anni intorno alla seconda guerra mondiale, vedeva nel suo apparecchio essenzialmente un mezzo mediante il quale sottrarre all’organismo del malato quanta più urea possibile, e regolarizzarne la situazione elettrolitica, con con riduzione notevole della sintomatologia uremica e miglioramento delle condizioni generali, in modo da consentire la sopravvivenza del paziente affetto da uremia acuta sino alla ripresa di una diuresi soddisfacente alle necessità metaboliche.
Si può afferrare che, nonostante i progressi compiuti dalla tecnica, questo concetto, che vede nel rene artificiale semplicemente un mezzo “eroico” da applicare singolarmente in determinate circostanze per permettere all’organismo di superare un particolare momento critico, è stato sino a pochi anni fa l’unico valido, senza notevoli modificazioni. Infatti i primi tentativi compiuti per introdurre la terapia emodialitica nel trattamento dell’insufficienza renale cronica si erano conclusi con un insuccesso, ed avevano portato ad esprimere pareri sostanzialmente negativi in proposito. Questa situazione si è ora radicalmente modificata, grazie soprattutto all’esperienza compiuta a Seattle da Scribner e coll., che si sono valsi di dializzatori a piccolo contenuto di sangue e bassa resistenza, ed all’adozione dello shunt artero-venoso in Teflon-Silastic (Quinton), che permette incannulazioni di lunga durata (oltre un anno) perfettamente tollerate dal paziente. Si è così formato il concetto di “emodialisi cronica” o “emodialisi periodica”, cioè di un trattamento a mezzo rene artificiale dell’insuffirenale cronica. Mediante un trattamento del genere si è dimostrato possibile sottrarre periodicamente ai pazienti cronici le sostanze responsabili della sindrome uremica, riportare di volta in volta il quadro chimico ed elettrolitico, se non alla norma, almeno ad un soddisfacente equilibrio, e permettere quindi a questi pazienti una sopravvivenza teoricamente indefinita. Naturalmente l’intrapresa di un trattamento del genere ha suscitato problemi clinici, tecnici ed organizzativi di notevole entità. Basti ricordare a questo proposito che un rene artificiale è in genere sufficiente ad appena due pazienti, mentre il fabbisogno della popolazione è notevolmente elevato, come pure elevati sono gli oneri finanziari annui a carico del paziente stesso e del centro emodialitico. Nonostante questi problemi, solo parzialmente risolti, questo tipo di trattamento è ormai uscito dalla prima fase sperimentale, ed attualmente si assiste ad una rapida diffusione di centri attrezzati per 1’emodialisi di pazienti affetti da insufficienza renale cronica.
Secondo statistiche fornite dall’European Dialysis and Transplant Association al congresso tenutosi a Dublino nel Giugno 1968, sono attualmente esistenti in Europa 114 centri attrezzati per il trattamento emodialitico dell’insufficienza renale cronica, per un totale di 1281 pazienti. L’incremento nel numero dei centri e dei pazienti trattati è stato, negli anni tra il 1965 ed il ‘68, notevolissimo, come si può osservare dalle tabelle N.1-2, e di per sé testimonia il successo ottenuto da questo tipo di trattamento dell’uremia cronica.
------Tabella n° 1------------------------------------------------------------------Tabella n° 2
R.D.T, in Europe (1965-68)--------------------------------------------------R.D.T. in Europe (1965-68)
Numero dei centri-------------------------------------------------------------Numero dei pazienti
1965---------43--------------------------------------------------------------1965---------160
1966---------54--------------------------------------------------------------1966---------295
1967---------81--------------------------------------------------------------1967---------621
1968--------11414-----------------------------------------------------------1968--------1281
Scopo della presente tesi è una messa a punto del problema dell’emodialisi periodica, sotto i suoi principali aspetti clinici, tecnici ed organizzativi, sulla base di 12 mesi di trattamento compiuti nella Clinica Medica dell’Università di Torino.
IL PRINCIPIO DEL RENE ARTIFICIALE –
I1 funzionamento del rene artificiale è basato sul principio della dialisi, per cui molecole e ioni in soluzione vengono separati da un sol colloidale. Si tratta cioè della capacità dell’acqua e dei cristalloidi di attraversare particolari membrane (di acetato di cellulosa, cellophane, cuprofano) impermeabili ai colloidi, membrane che separano due compartimenti, nel primo dei quali circola il sangue del paziente, mentre nell’altro si trova una particolare soluzione, variabile a seconda delle circostanze nella sua composizione, che costituisce il bagno di dialisi. Il passaggio dell’acqua e dei cristalloidi attraverso queste membrane avviene secondo la legge di Donnan, e tende al raggiungimento di un equilibrio nei due settori.
I primi passi verso l’ideazione di un apparecchio con queste caratteristiche vennero compiuti nel 1913 da Abel, Rowentree e Turner, i quali coniarono il termine di “artificial kidney”. I successivi lavori di Necheles, Thalhimer etc., non ebbero tuttavia seguito, ed il primo a raggiungere una realizzazione pratica ed a compiere esperienze cliniche col nuovo apparecchio fu Willem J. Kolff, olandese, negli anni tra il 1940 ed il ‘45. I1 primo rene artificiale era costituito essenzialmente da un tubo di cellophane lungo 20 metri, avvolto a spirale attorno ad un rullo orizzontale immerso per la metà inferiore in una vasca di liquido dializzante. Facendo ruotare il rullo su se stesso il sangue contenuto nel tubo, ove era stato introdotto dopo essere stato prelevato al paziente, era forzato per gravità a spostarsi da un capo all’altro del tubo stesso seguendone la parte inferiore immersa nel liquido. Successivamente esso veniva restituito a1 paziente.
I notevoli successi pratici ottenuti con questo prototipo furono rapidamente seguiti da migliorie tecniche dell’apparecchiatura, sì che oggi è disponibile una vasta gamma di dializzatori con differenti caratteristiche ed indicazioni all’impiego.
Caratteristiche del dializzatore ideale.
Le caratteristiche del dializzatore ideale per il trattamento dei pazienti uremici cronici sono considerate da Freeman, Naher e Schreiner essere le seguenti:
a) Innanzitutto il dializzatore deve possedere un elevato potere depuratore nei confronti dell’azoto ureico e degli altri prodotti tossici propri del metabolismo dell’uremico. La misura di questo potere, cioè il rendimento del dializzatore in esame viene espresso da Wolf e coll. in termini di ‘dialisance”: essa fornisce una misura della quantità di un dato soluto che viene rimossa dal dializzatore, in relazione al livello ematico dello stesso e costituisce quindi un’efficace unità di misura funzionale, paragonabile alla clearance renale. Per mezzo di essa possono quindi venir raffrontati criticamente i diversi apparecchi emodialitici. La dialisance viene espressa dalla seguente formula secondo Wolf, Kemp, Kiley e Curie:
--------A-B
D = a -----
--------A-U
in cui a esprime il flusso sanguignio attraverso l’apparecchio (in cc./minuto); A = concentrazione della sostanza nel sangue all’ingresso; B = concentrazione del la medesima sostanza nel sangue all’uscita, e U concentrazione nel bagno di dialisi. E’ chiaro come un’elevata díalisance nei confronti delle sostanze responsabili della sindrome uremica. e specialmente dell’urea, sia una caratteristica indispensabile di un buon apparecchio dializzatore. D’altra parte Freeman e coll. sottolineano come una troppo rapida rimozione di soluti dall’organismo non è neppur essa auspicabile, potendo risolversi in quella che è stata definita “disequilibrium syndrome”, caratterizzata clinicamente da vomito, alterazioni dei valori pressori, cefalea, nausea, disturbi mentali etc,
b) E’ preferibile che il dializzatore offra una bassa resistenza interna al passaggio del sangue, in modo che esso possa essere spinto nel circuito dalla sola pressione arteriosa del paziente, eliminando la necessità di una pompa e rendendo il trattamento più sicuro e meno traumatizzante.
c) I1 dializzatore ideale deve avere un volume interno ridotto. Nei dializzatori ad alto volume si rende infatti necessario riempire il circuito prima di ogni applicazione con sangue di donatori, il che, a lungo andare, può portare ad una sensibilizzazione del paziente, richiede l’uso di quantità elevate di eparina e nasconde sempre il pericolo di infezioni epatitiche.
d) Un’altra caratteristica importante è 1a capacità di rimuovere acqua e liquidi da pazienti oligurici ed iperidratati. L’entità di questa rimozione è in dipendenza della sottigliezza delle membrane che separano il sangue dal bagno di dialisi e della loro porosità. Per accrescere il tasso di filtrazione si può ricorrere a svariati accorgimenti, quali l’aumentare il gradiente di pressione ai due lati della membrana dializzante cosa che può essere ottenuta sia elevando la pressione idrostatica del sangue nell’apparecchio, sia esercitando un’aspirazione sul liquido di dialisi, creando cioè una pressione negativa nell’opposto settore. Un terzo sistema consiste nell’aumentare 1’osmolarità del liquido di dialisi accrescendone il contenuto ad esempio in glucosio.
e) Infine il circuito interno dell’appareccchio ed i tubi connettori debbono preferibilmente essere pronti e presterilizzati, sicuri e di poco costo.
Nessun tipo di rene artificiale attualmente esistente possiede al completo le suesposte caratteristiche, ma solo alcune di esse, il che rende l’uno o l’altro apparecchio preferibile nei vari casi e nelle diverse circostanze. Si possono in definitiva distinguere da una parte dializzatori a grande capacità (da 1 litro a 3 litri di volume interno), rappresentati essenzialmente dallo “standard Twin coil”, dall’altra quelli a piccola capacità (volume interno sino a 500-600 cc.) e cioè il “cronic coil” ed i dializzatori a strati paralleli Skeggs-Leonard, Kiil, Dialung-Esmond e AB Gambro.
Le caratteristiche tecniche di questi apparecchi sono riportate nella seguente tabella riassuntiva, parzialmente riportata da Freeman e coll.:
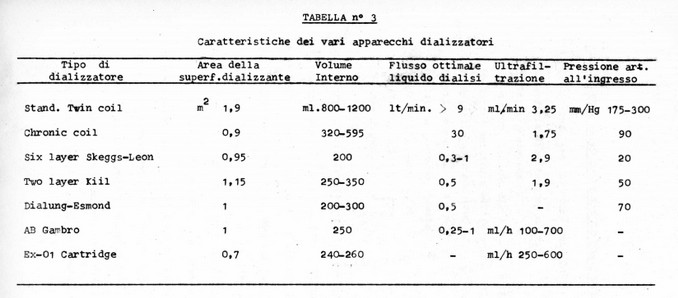
TIPI DI RENE ARTIFICIALE E LORO CARATTERISTICHE
1) Il dializzatore "Standard Twin Coil”
---Superficie dializzante m 1.9
---Dialisance elevata
---Flusso ott. liquido dialisi : > 9 lt/min.
---Pressione arteriosa all’ingresso : 170mm/Hg
---Volume interno : 800ml
---Pre-riempito con sangue : sì
---Resistenza interna elevata
---Pompa per il sangue : si
---Durata dialisi : 5-6 ore
---Presterilizzato
Questo tipo di dializzatore ha il vantaggio che l’unità filtrante. cioè la cartuccia (coíl) di Ko1ff e Watchinger, è ottenibile in commercio già pronta e presterilizzata. Essa è formata da due tubi paralleli di cellulosa avvolti attorno ad un sostegno centrale in Fiberglass, lunghi ciascuno 10,85 m. e con una superficie totale dializzante elevata (m2 1,9). Gli svantaggi di questo tipo di rene sono rappresentati dall’elevato volume interno, che richiede un preventivo riempimento con sangue, e dall’alta resistenza del circuito, che rende necessario l’uso di una pompa ematica. Se questi inconvenienti ne limitano le possibilità d’impiego in un programma di emodialisi periodica, tuttavia l’elevata capacità depuratrice di questo apparecchio lo rende il mezzo di scelta in situazioni di emergenza, quali casi urgenti di uremia acuta o con elevati livelli azotemici.
2) Chronic Coil Dializer
---Superficie dializzante : m2 0,9
---Dialisance discreta
---Flusso ott. liquido dialisi : 30 lt/min.
---Pressione arteriosa all’ingresso : 90 mm/Hg
---Volume interno : 320-595 ml
---Preriempimento con sangue : no
---Resistenza interna media
---Pompa per il sangue : no
---Durata dialisi : 8-12 ore
---Presterilizzato
Si tratta di una modificazione del precedente, attuata dai laboratori Travenol, al fine di renderlo più adeguato alle richieste per un trattamento emodialitico perioa lunga scadenza. La lunghezza di ciascuno dei due tubi di cellulosa della cartuccia filtrante è stato ricirca della metà (m. 5,2), mentre è stato aumentato il diametro del cilindro cavo di sostegno. I1 volume interno ne risulta diminuito, e così pure diminuite sono le resistenze interne del sistema. Ai vantaggi codall’abolizione della pompa per il sangue e di un preventivo riempimento si contrappone però una ridotta efficienza dell’apparecchio (conseguenalla diminuzione della superficie filtrante), che si traduce nella necessità di applicazioni di più lunga durata. Secondo quanto riferiscono Freeman e coll. l’efficienza di questo tipo di dializzatore è di molinferiore a quella dello Standard Twin Coil ed equivale ai 2/3 di quella del rene Kiil.
Sia per il Chronic che per lo Standard Coil, un accorgimento utile per eseguire successive dialisi senza ricorrere ogni volta al riempimento del circuicon sangue di donatore è quello di effettuarne il recupero al termine della dialisi e riutilizzarlo poi nella successiva; questa metodica, definita da Hansson e coll. “autotrasfusione”, non è però scevra di inconquali il pericolo di infezioni epatitiche e di una sensibilizzazione del paziente.
3) I1 rene artificiale Skeggs
---Superficie dializzante : m2 0,95
---Dialisance bassa
---Flusso ott. liquido dialisi : 0,3-1/lt
---Pressione arteriosa all’ingresso : 20 mm/Hg
---Volume interno : 200 ml
---Preriempimento con sangue : no
---Resistenza interna bassa
---Pompa per il sangue : no
---Durata dialisi : 12 ore
---Necessita preparazione e sterilizzazione
Si tratta di un apparecchio a piccola capacità, in cui il sangue circola in strati paralleli tra speciali fogli di cellophane che costituiscono la membrana dializzante. I1 modello più usato è costituito da sei strati. La basresistenza interna e la piccola capacità costituiscoi vantaggi dì questo tipo di rene artificiale. Ad essi contrappongono pero numerosi inconvenienti. Innanl’apparecchio richiede una preparazione complicata e lunga (da 2 a 4 ore), nonché un rigoroso collaudo prima di ogni applicazione. A ciò si deve aggiungere la necessità di una sterilizzazione a freddo mediante ze(cloruro di benzalkonio), sostanza inattiva conil virus epatitico, poiché il sangue viene a contatto anche con parti in metallo e gomma, che devono venisiliconate per prevenire la formazione di coaguli. Infine le prove di dialisance indicano lo Skeggs come l’apparecchio meno efficiente dal punto di vista della rimozione dei vari soluti.
4)- dializzatore Kiil (Figura n° 1)
---Superficie dializzante : m2 1
---Dialisance buona
---Flusso ott. liquido dialisi 500 ml/min.
---Pressione arteriosa all’ingresso: 50 mm.Hg
---Volume interno : 250-350 ml
---Preriempimento con sangue : no
---Resistenza interna bassa
---Pompa per il sangue : no
---Durata dialisi : 10-12 ore
---Necessita preparazione e sterilizzazione.
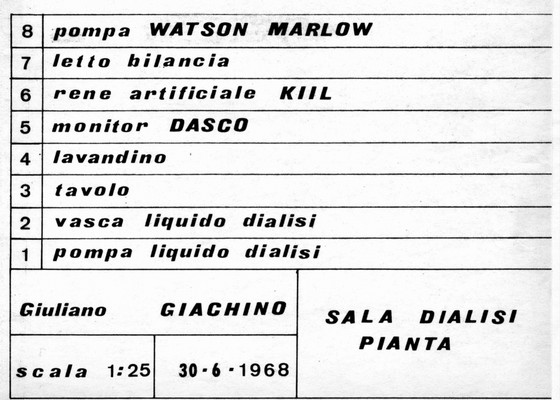
Si tratta dell’apparecchio che si è dimostrato uno dei più adatti per il trattamento della insufficienza renalecronica mediante dialisi periodica, ed è quello che viene abitualmente utilizzato a questo scopo nella Clinica Medica dell’Università di Torino. Anche in questo apparecchio il sangue scorre in strati paralleli (2 o 3 a seconda del tipo di apparecchio), tra due membrane di cuprofano, che lo separano dal liquido di dialisi che scorre in direzione opposta. Le strutture di sostegno sono rappresentate da piastre rettangolari in materiale plastico o plexiglass (Dasco).
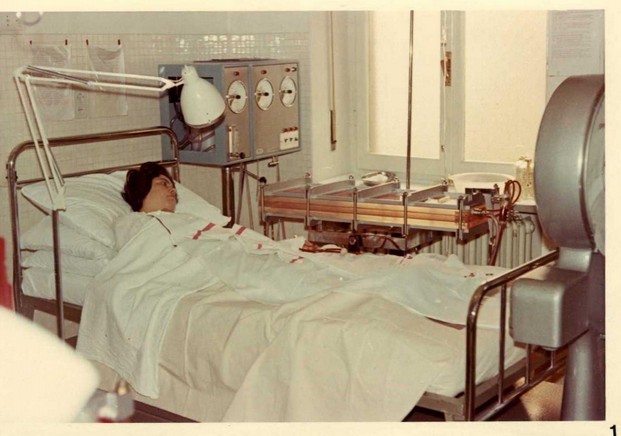
Figura n° 1. Veduta parziale della sala dialisi con letto-bilancia e dializzatore Kiil
E’ da sottolineare come, nel Kiil, a differenza dello Skeggsil sangue del paziente entri in contatto esclusivamente con parti che non vengono riutilizzate, (e che si riducono essenzialmente alle derivazioni di entrata e di uscita ed alle membrane dializzanti), riducendo così di molto il pericolo di reazioni da pirogeni e di eventuali trasmissioni di affezioni virali. Le piastre sono realizzate in polipropilene oppure in plexiglass trasparente poiché in tal modo presentano i vantaggi seguenti :
a) Possibilità di controllo visivo dell’uniforme distribuzione del sangue nel circuito. b) Possibilità di controllo visivo dell’eparinizzazione regionale. c) Possià di controllare (bolle d’aria) il passaggio del liquido dializzante. d) Controllo del circuito del sangue allorché, al termine della dialisi, si restituisce al paziente il sangue contenuto nell’apparecchio. e) Un migliore controllo delle condizioni di pulizia dell’apparecchio.
I1 volume interno assai ridotto del Kiíl rende superfluo il preventivo riempimento del circuito con sangue di donatore e rende ciò effettuabile all’inizio dell’applicazione mediante il sangue del paziente stesso, a cui sarà successivamente reinfuso al termine della stessa. La bassa resistenza permette di abolire la pompa per il sangue, raggiungendosi anche senza di essa dei flussi ematici del l’ordine di 200 ml/min. La superficie dializzante discretamente elevata conferisce all’apparecchio un buon potere depuratore nei confronti dei vari soluti. La misurazione della dialisance ureica eseguita da Confortini in svariate condizioni di funzionamento conferma l’efficienza del rene Kiil sotto questo punto di vista, come si può vedere dalla seguente tabella (da Confortini e coll.)
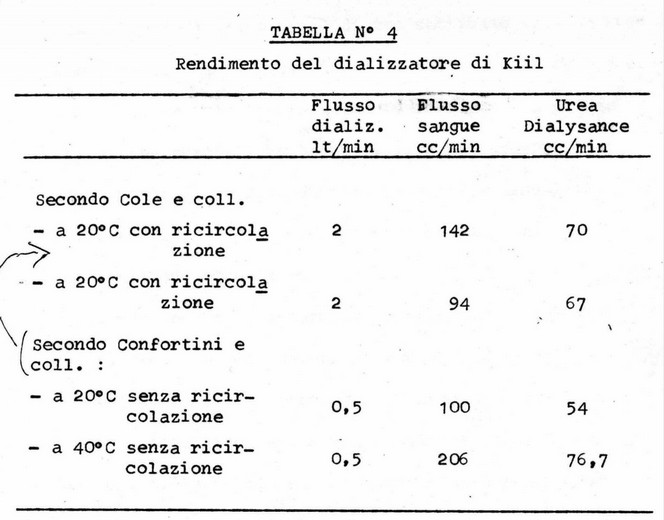
Il dializzatore Kiil presenta esso pure alcuni inconvenienti. Essi sono rappresentati dalla necessità di dialisi di lunga durata (sino a 12 ore) e del fatto di non possedere le caratteristiche di presterilizzazione. I1 fatto che questo rene debba venire preparato e sterilizzato prima dell’uso lo rende ovviamente inadatto nelle situazioni di emergenza, ma si deve osservare che una volta pronto e riempito con la soluzione disinfettante esso può essere lasciato a sé come riserva anche per lunghi periodi (sino a più di tre settimane secondo Freeman), senza che si osservino alterazioni delle membrane. Sono inoltre attualmente allo studio ed in via di realizzazione speciali membrane dializzanti presterilizzate e pronte all’uso, mediante le quali le manualità di preparazione del rene Kiil verranno notevolmente semplificate ed abbreviate.
L’apparecchiatura tecnica accessoria al rene Kiil che ci viene fornita dai Laboratori Dasco è composta inoltre da un riscaldatore del liquido di dialisi, un circuito idraulico, una pompa di ultrafiltrazione e dal monitor, mediante il quale possono venire controllati in ogni istante la temperatura, la pressione ed il flusso del liquido, nonché la pressione del sangue nel dializzatore.
Un’interessante modificazione del rene Kiil è quel la studiata da Monasterio e coll. nella Clinica Medicai dell’Università di Pisa, e che consiste nel portare da due a tre i compartimenti dializzanti del rene, aumentandone la superficie dializzante del 50%. Questa modificazione, suggerita inizialmente dalla necessità di trattare alcuni pazienti di notevole dimensione corporea ha come conseguenza un notevole aumento dell’efficienza dialitica, che rende possibile anche in questi pazienti una depurazione ematica di entità eguale a quella che si ottiene nei malati di minori dimensioni. L’uso del rene Kiil a tre compartimenti dializzanti non ha rivelato la comparsa di alcun disturbo collaterale legato alla sua maggiore capacità (285 ml contro 208 ml in media), e può quindi essere consigliato, per la sua maggiore efficienza, in tutti i pazienti che intraprendono la terapia dialitica cronica.
Si può quindi concludere affermando che in complesso il dializzatore tipo Kiìl, pur non possedendo tutte le caratteristiche richieste, si avvicina soddisfacentemente al modello ideale per una dialisi di tipo periodico e può anzi sostenere talvolta buona prova anche nel trattamento di certuni casi di uremia acuta
5) I1 rene Dialung-Esmond
---Superficie dializzante : m2 1
---Dialisance elevata
---Flusso ott. liquido dialisi : 500 ml/min.
---Pressione arteriosa all’ingresso : 70 mmHg.
---Volume interno : 200-300 ml.
---Preriempimento con sangue : no
---Resistenza interna bassa
---Pompa per il sangue : no
---Durata dialisi : 10-12 ore
---Necessita preparazione e sterilizzazione.
Questo dializzatore consiste di 65 piastre rettangolari di polipropilene alternate a membrane di cuprofano, ed unite alle estremità da due piastre in lexan rinforzata con fibre di vetro. I1 vantaggio fondamentale di questo tipo di rene artificiale è rappresentato dalle ridotte dimensioni e dal minimo ingombro: l’apparecchio completo, con superficie dializzante di 1 m2, misura infatti cm. 20x20x13 e pesa 4,7 Kg. Questo apparecchio inoltre non richiede l’uso di una pompa per il sangue, né il preventivo riempimento del circuito ematico poiché le resistenze interne sono molto basse (flusso ottenibile di 200 ml di sangue al minuto con una pressione arteriosa di 70 mmHg.), ed il volume interno ridotto. La dialisance di questo apparecchio è notevolmente elevata: 700 ml/min. per un flusso sanguigno di 200 ml/minuto. L’apparecchio richiede preparazione e sterilizzazione, che si può eseguire mediante acido acetico al 4%, zephiran ed ossido etilene, ma date le sue ridotte dimensioni ciò non rappresenta uno svantaggio di eccessiva entità. Queste caratteristiche, unite al costo relativamente basso del trattamento, fanno del Dialung-Esmond un apparecchio discretamente indicato per il trattamento ospedaliero ed a domicilio dell’insufficienza renale cronica.
6) Il rene AB Gambro.
---Superficie dializzante : m2 1
---Dialisance elevata
---Flusso ott. liquido dialisi: 0,25-1 lt/min.
---Pressione arteriosa all’ingresso:
---volume interno : 250 ml.
---Preriempimento con sangue : no
---Resistenza interna bassa
---Pompa per il sangue : no
---Durata dialisi : 6 ore
---Pronto per l’uso. Non riutilizzato.
I vantaggi principali di questo nuovo tipo di rene artificiale sono rappresentati dal fatto che la parte filtrante viene messa in commercio già presterilizzata e pronta per l’uso e non viene riutilizzata per successive applicazioni. Inoltre la notevole capacità depuratrice dell’apparecchio e l’elevato flusso del liquido dializzante permettono di ridurre la durata di ogni singola applicazione a circa sei ore. A questi vantaggi esclusivi di questo tipo di rene vanno aggiunti quelli in comune con il Kiil ed il Dialung-Esmond, quali la bassa resistenza del circuito ed il ridotto volume interno che eliminano la necessità di una pompa ematica e di un preventivo riempimento con sangue di donatore.
Come si è visto quasi tutti questi tipi di rene artificiale - tranne lo Standard Twin Coil, il Chronic Coil ed il rene AB Gambro, le cui cartuccie filtranti sono messe in vendita dalle case produttrici già pronte per l’uso, richiedono preparazione e sterilizzazione.
La tecnica originale di Scribner per la sterilizzazione degli apparecchi emodialitici ha rivelato alcuni inconvenienti. Essa prevedeva la sterilizzazione dei serbatoi centrali del liquido dializzante a mezzo di detersivi ed ipoclorito e quella del dializzatore mediante cloruro di benzalkonio (Zephiran). Ora, mentre gli ipocloriti non garantiscono un sufficiente grado di sterilizzazione, lo zephiran è una sostanza tossica anche in piccola quantità per l’organismo e richiede quindi un abbondante e prolungato lavaggio al fine di eliminare completamente ogni traccia. Esso inoltre, come si è già detto, è inattivo nei confronti del virus dell’epatite da siero. Altre sostanze prese via via in considerazione sono state l’acido acetico al 3% e l’alcool etilico al 70%. ma quest’ultimo senza risultati soddisfacenti.
La sostanza di cui si fa abitualmente uso a questo copo nel centro emodialitico della Clinica Medica dell’Universìtà di Torino è la formalina in soluzione acquosa al 4%, La preparazione viene effettuata nella farmacia dell’Ospedale utilizzando acqua distillata apirogenica, il che ha annullato l’incidenza dì reazioni pirogeniche. I vantaggi della formalina sano il costo bassissimo, la buona efficienza sterilizzatrice con attività verso i germi, le spore, i funghi ed i virus, accompagnata da una scarsa tossicità, infine Confortini (da Johnson) sottolinea come la formalina inattivi eventuali tossine presenti trasformandole in tossoidi non pericolosi.
I1 bagno di dialisi-
L’importanza di una corretta composizione del liquido di dialisi ai fini di una buona efficienza del trattamento e di un regolare svolgimento dello stesso non può. essere sopravalutata. I1 passaggio dei vari ioni attraverso le membrane dializzanti nel senso sangue-liquido di dialisi ed in quello opposto è regolato nella sua velocità ed entità dalle leggi di Donnan e della elettroneutralità. La prima afferma che, ad equilibrio raggiunto, i prodotti delle concentrazioni degli joni diffusibili sono eguali nei due opposti compartimenti; per la seconda la somma degli joni positivi eguaglia quella degli joni negativi da entrambi i lati.
La presenza basale di alcuni elementi e composti, quali il sodio, il potassio, il calcio, il magnesio, bicarbonati, cloruri e glucosio è indispensabile al fine di evitare una loro deplezione nell’organismo. Ovviamente la loro concentrazione nel bagno potrà venire opportunamente variata a seconda delle necessità contingenti nel caso specifico. Ad esempio è stato dimostrato che mantenendo la concentrazione del sodio nel bagno ad un livello inferiore a quello ematico (125-135 mEq/l), cioè provocando un certo grado di deplezione dì questo sale, ed associando a questo trattamento un adeguato grado di ultra. filtrazione si può ottenere un buon controllo degli stati ipertensivi che abitualmente accompagnano l’insufficienza renale cronica.
Allo stesso modo, mantenendo la concentrazione dello jone potassio a valori di 2-205 mEq/lt. si può rimuovere mediante dialisi l’eccesso di potassio derivante dalla sua diminuita escrezione e mantenere la kaliemia entro limiti normali.
Come è stato già precedentemente sottolineato un utile accorgimento al fine di accrescere la sottrazione di liquidi è quello di aumentare 1’osmolarità del bagno, rendendolo ipertonico per mezzo di un alto contenuto in glucosio (ultrafiltrazione chimica).
In definitiva la composizione del bagno di dialisi deve venire opportunamente modificata a seconda delle circostanze e delle necessità particolari dei diversi pazienti; è opportuno ai fini di una corretta metodica prendere in considerazione anche la possibile presenza - talvolta in quantitativi non trascurabili - di alcune sostanze quali alcali, cloro, magnesio, nell’acqua di distribuzione abitualmente utilizzata, e le loro possibili variazioni stagionali e geografiche.
Attualmente, nonostante l’ideale sia rappresentato dal bagno di dialisi a composizione particolare per ogni determinato paziente, si tende in genere, per motivi di praticità e comodità, ad approntare dei bagni a composimedia confacentisi alle richieste di circostanze diverse tra di loro.
Per quello che riguarda le modalità di preparazione del bagno di dialisi si hanno tre possibilità:
1) Preparazione estemporanea a partenza da sali che vengono sciolti nell’acqua. Si tratta di un sistema pratico, ma che nasconde la possibilità di errori anche assai gravi (caricamento doppio dei sali, dimenticanza di alcuni di essi). In alcuni casi in cui detti errori sono stati commessi le conseguenze sono siate purtroppo letali per i pazienti. A detti errori è possibile ovviare mediante determinazioni fotometriche della composizione del liquido di dialisi o per mezzo di osmometri bloccanti l’afflusso del liquido stesso alle pompe di distribuzione.
2) Preparazione estemporanea a partenza da soluzioni concentrate e tarate. Questa metodica ha il vantaggio di evitare numerose pesate dei salì e si presta particolarmente per servizi di notevole entità.
3) Adozione di apparecchi mescolatori automatici a partenza da soluzioni concentrate. Un esempio di questo tipo di apparecchio è quello realizzato dalla Joseph Lucas Electrical Ltd. Questo apparecchio, altamente automatizzato, produce il liquido di dialisi partendo da una soluzione concentrata che diluisce con acqua nella proporzione di 1 a 35, e controlla l’esatta composizione del liquido ottenuto misurandone la conduttività elettrica.
La tendenza attualmente prevalente è quella di adottare mescolatori centralizzati in grado di fornire il liquidi di dialisi ad un elevato numero di reni artificiali contemporaneamente.
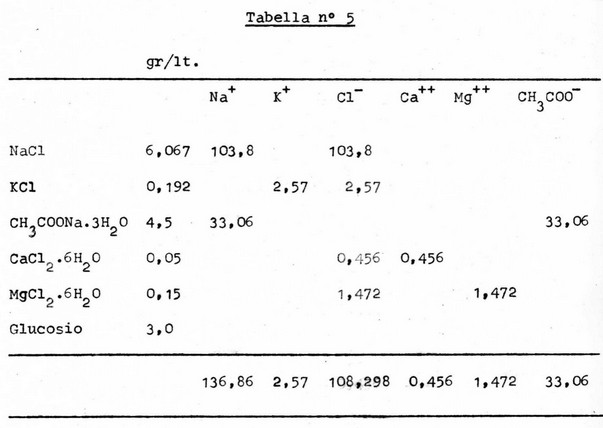
Nel caso si faccia uso del primo dei tre metodi precedentemente illustrati, e indispensabile procedere, prima di ogni singola dialisi, alla determinazione laboratoristica del contenuto dei principali elettroliti. E’ qui riportata a titolo di esempio (Tabella n° 5), la composizionedel bagno di dialisi da noi attualmente utilizzato:
ALLACCIAMENTO AL PAZIENTE
Un problema di fondamentale importanza si è rivelato sin dalle prime esperienze col rene artificiale, il sistema di allacciamento dell’apparecchio dializzatore al paziente.
Inizialmente Kolff prelevava il sangue al paziente, lo immetteva nell’apparecchio e quindi lo ritrasfondeva, ripetendo l’operazione sino a raggiungere un adeguato volume di sangue. In seguito modificò 1’operazione adottando un ciclo continuo, collegando cioè durante la dialisi il paziente all’apparecchio mediante una linea arteriosa ed una venosa facenti capo ad aghi e facendo uso di eparina per impedire la coagulazione. Un passo successivo fu rappresentato dall’incannulamento dell’arteria radiale con tubi di vetro, plastica ed altri materiali meno traumatizzanti e più resistenti.
Mediante 1’incannulazione vasale, il rene artificiale può essere collegato al malato in due modi: utilizzando un sistema vena-vena oppure arteria-vena. Nel primo caso, in cui è implicita la necessità di una pompa per il sangue, vengono ordinariamente utilizzate la vena cava, raggiunta tramite esposizione chirurgica della safena interna, ed una vena di un arto superiore. Nel secondo, arteria-vena che fu quello già seguito da Koiff ed Alwall, vengono generalmente utilizzate l’arteria radiale ed una vena di un arto superiore, ma anche l’ulnare e la tibiale posteriore si prestano pure allo scopo. Questo sistema di incannulamento è tuttavia praticamente incompatibile con un trattamento emodialitico prolungato. Una simile metodica infatti, per quanto perfezionata negli ultimi anni, vede il suo limite nel numero di applicazioni da effettuare, in quanto le possibili sedi di inserzione delle cannule vengono in breve esaurite.
Un simile inconveniente, già notevole nei casi di applicazione del rene artificiale ai malati acuti, è ovviamente più grave e praticamente insormontabile da un programma di emodialisi periodica nei malati cronici, con applicazioni ripetute e ad indefinita scadenza. Questo problema è stato solo recentemente risolto mediante una incannulazione permanente arterodefinita dai suoi ideatori “shunt" o "by-pass” artero-venoso.
Shunt -
L’incannulazione permanente dei vasi ai fini del1’emodialisi è stata per primi realizzata da Quinton, Dillard e Scribner nel 1960 a Seattle (Washington, U.S.A.), utilizzando tubi in teflon, una sostanza ben tollerata dall’organismo. Due cannule di detta sostanza inserite rispettivamente in un’arteria ed in una vena, dopo un breve percorso sottocutaneo perforano la cute emergendo all’esterno, e nell’intervallo tra una dialisi e l’altra sono tra di loro connesse dando origine ad un corto circuito artero-venoso continuo extra corporeo. Nell’originale prototipo di Quinton i due tubi in teflon erano tra di loro uniti da un segmento in teflon foggiato ad U, che veniva rimosso allorché si procedeva alla dialisi e reinserito al termine della stessa. Molti lavori riportano i notevoli inconvenienti dovuti alla rigidità di questo sistema, riassumibili essenzialmente nel pericolo di lesioni dell’estremità vasale incannulata e dei punti di emergenza della cute causate da trazioni conseguenti a movimenti dell’arto del paziente, a traumatismi od alle stesse manipolazioni mediche.
Questa protesi vasale è stata successivamente modificata dai medesimi autori in questo senso:
1) ntroduzione del sistema in Silastic. L’inserzione di un segmento in Silastic, materia flessibile, tra il tratto in teflon inserito nel vaso e quello esterno ha consentito ad ovviare a gran parte degli inconvenienti presentati dal tipo originale di shunt, interamente in teflon. E’ attualmente reperibile in commercio una vasta gamma dì cannule in Silastic, prodotto principalmente dalla Quinton Company e dalla Extracorporeal.
2) Abbandono degli anelli metallici di giunzione. Inizialmente la porzione in silastic era saldamente ancorata alle sezioni in teflon mediante anelli metallici a pressione; detti anelli sono stati sostituiti con legature in seta, meno ingombranti e traumatizzanti.
3) Abbandono della giunzione ad U e sua sostituzione con un breve ponte rettilineo in teflon di 2 cm di lunghezza.
Lo shunt di Quinton modificato (Figura N° 2) viene quindi a constare in ciascuna delle due sezioni, arteriosa e venosa di un segmento in teflon inserito nel vaso, e di un segmento in silastic a sua volta divisibile in tre parti, una interna che descrive nel sottocutaneo una curva di 180° circa, uno scalino verticale di 45° ed una parte esterna che emerge quindi dalla cute in direzione prossimale. Questa disposizione ha il vantaggio di presentare un punto di emergenza dello shunt attraverso la cute lontano dal punto di inserzione vasale (minimizzazione dei pericoli di infezione, flebite, trombosi), e lo scopo di evitare che la parte sottocutanea dello shunt stesso, circondata da tessuto cicatriziale, possa accidentalmente sfilarsi in seguito a trazione od alla continua sollecitazione determinata dalle pulsazioni vasali.
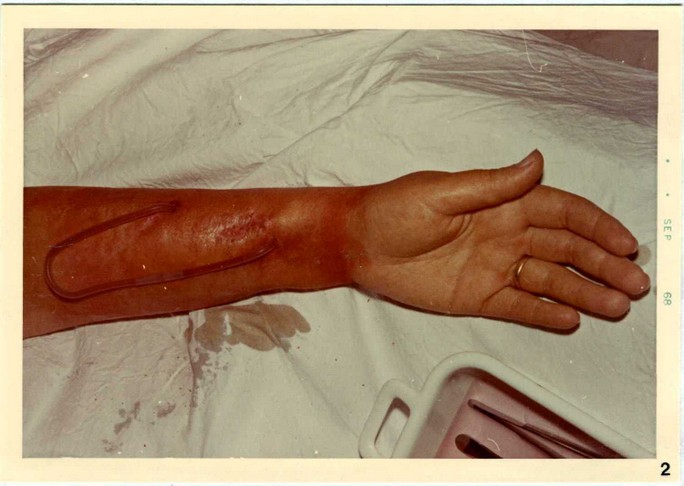
Figura N° 2 - Shunt curvo di Scribner e Quinton.
Un’ultima modificazione dello shunt artero-venoso - chiamato diritto, in confronto a precedente curvo è quella apportata da Ramirez : in questo tipo di shunt (Figura N° 3) la porzione sottocutanea non descrive alcuna curva ed il pericolo di distacco è evitato da un ancoraggio chirurgico alla massa cicatriziale. Detto ancoraggio possibile dalla presenza, sulla superficie del segmento in silastic sottocutaneo, di due piccole alette trettangolari della medesima sostanza. I vantaggi dello shunt diritto sono riassumibili essenzialmente in una maggiore facilità di impianto e nel caso di formazione di coaguli di una più semplice tecnica di disostruzione.
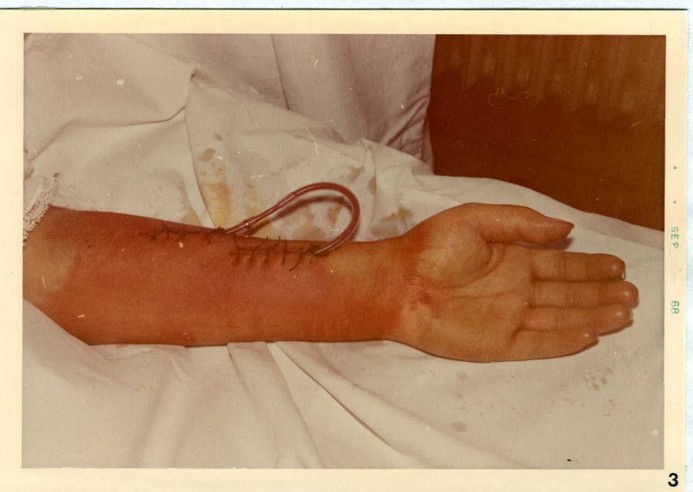
Figura N° 3 - Shunt diritto di Ramirez
I1 luogo abitualmente prescelto per l’inserzione dello shunt è 1’avambraccio sinistro nei destrimani. I vasi più frequentemente utilizzati sono le arterie radiale od ulnare ed ogni vena di sufficiente calibro, ad esempio la cefalica o la basilica. Lo shunt può anche essere inserito col risultato di consentire al paziente un più libero uso delle braccia, agli arti inferiori, come riportato da numerosi autori; in questo caso i vasi utilizzati più frequentemente sono l’arteria tibiale posteriore e le vene safena interna ed esterna (Figura N° 4). L’inserzione dello shunt negli arti inferiori è stata inizialmente eseguita in pazienti nei quali in seguito a vari successivi trasferimenti dello shunt stesso, non erano più utilizzabili vasi delle estremità superiori; oggi la si esegue correntemente in pazienti che debbano svolgere un’attività lavorativa manuale o che eseguano la dialisi a domicilio. Keon e coll. hanno utilizzato anche in un caso l’arteria epigastrica inferiore ed una vena addominale.
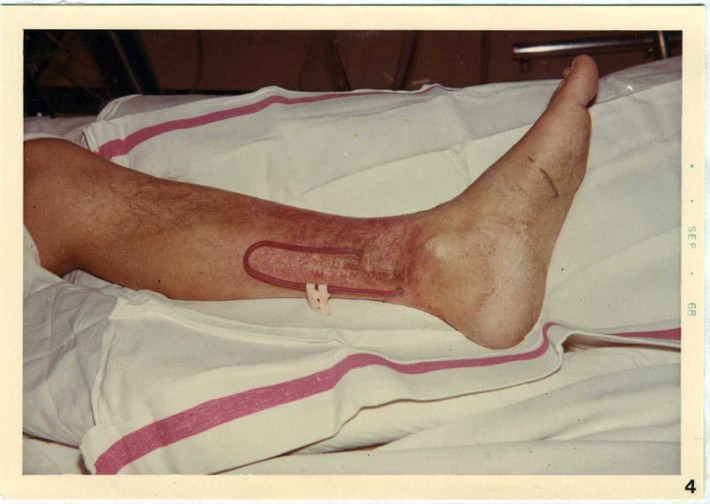
Figura N° 4 - Shunt curvo di Scribner e Quinton inserito nella gamba sinistra
L’inserzione degli shunts richiede un intervento di chirurgia vascolare in anestesia locale; alcuni autori consigliano l’anestesia del plesso brachiale al fine di evitare ogni movimento dell’arto durante l’intervento ed alterazione dei rapporti anatomici delle parti in seguito ad iniezione locale di anestetico. Nella nostra Clinica l’inserzione viene eseguita secondo la tecnica proposta da Quinton e coll., la quale prevede due incisioni cutanee longitudinali separate, una per l’arteria e l’altra per la vena. Una particolareggiata descrizione dei vari tempi dell’intervento è riportata nei lavori di Yoffa e coll. Assai recentemente alcuni autori canadesi ed americani hanno proposto una modificazione di detta tecnica consistente nel praticare un’unica incisione cutanea tra i due vasi, anziché due, per l’esposizione dell’arteria e della vena, ed una successiva loro divisione in due separati compartimenti mediante una sutura sottocutanea; i vantaggi di questa tecnica sarebbe un ridotto tempo operatorio e diminuzione del rischio di infezione.
Lo shunt artero-venoso è concordemente indicato da quasi tutti gli autori come il punto debole dell’apparecchiatura tecnica dell’emodialisi. Gli inconvenienti e le complicazioni più frequenti degli shunts sono la coagulazione, l’infezione, l’erosione della cute sovrastante e l’accidentale apertura dello stesso. La coagulazione sanguigna all’interno dello shunt è universalmente ritenuta la complicazione più frequente ad osservarsi. Essa, generalmente più frequente nel settore venoso è denunciata da numerosi segni tra i quali il dolore, la scomparsa del fremito sistolico all’auscultazione sull’arteria incannulata, la diminuzione della temperatura, la decolorazione del contenuto delle cannule per eritrosedimentazione. I pazienti sono in genere allenati a riconoscere tempestivamente i segni rivelatori di questo fenomeno la cui causa immediata più frequente pare essere la diminuzione del flusso sanguigno attraverso lo shunt stesso. A sua volta questa diminuzione del flusso sanguigne può dipendere da varie cause quali improvvise cadute pressorie, compressioni dello shunt, endoarteriti, trombosi, etc.
L’infezione dello shunt può essere causa di complicazioni assai più gravi. Numerosi casi di setticemia anche mortale o difficilmente domata dagli antibiotici conseguente ad infezioni dello shunt sono riportati da Stille e coll., e casi di infezioni più lievi da quasi tutti gli autori. Ne consegue la necessità di una rigorosa asepsi durante l’inserzione e nelle successive manualità dì routine di apertura e chiusura degli shunt e specialmente dei loro punti di emergenza della cute -ove più facile è la penetrazione di germi, rappresentando essi una permanente soluzione di continuo.
Con una certa frequenza si può pure osservare protrusione all’esterno di porzioni sottocutanee dello shunt in seguito a necrosi ed erosione della cute sovrastante conseguente al costante cronico traumatismo determinato dalle pulsazioni dello stesso. Fenomeni di questo tipo sono ovviamente favoriti dalle infezioni o dalla presenza di parti metalliche (anelli), come si verificava con i tipi più primitivi di shunt. Un fattore concomitante può essere rappresentato, in questi casi, da un’atrofia sub-clinica dei tessuti circostanti insufficientemente irrorati in seguito alla presenza del corto-circuito artero-venoso e di un circolo collaterale non perfettamente vicariante.
L’apertura accidentale dello shunt è un evento assai raro. Tuttavia alcuni autori ne riportano alcuni casi, tra cui uno estremo di morte per dissanguamento.
Fistola arterovenosa -
Di fronte ai numerosi inconvenienti presentati dagli shunt artero-venosi artificiali, tra i quali non ultimi quelli di ordine psicologico da parte di numerosi pazienti che mal sopportano tale protesi permanente, Cimino e Brescia hanno dapprima proposto la semplice puntura venosa (1962), e quindi messo a punto un metodo che consente di eliminare lo shunt artificiale, creando chirurgicamente una fistola arterosottocutanea tra l’arteria radiale ed una qualsiasi adeguata vena dell’avambraccio.
I1 procedimento chirurgico proposto da questi autori si esegue in anestesia locale e prevede un’incisione laterale di circa 0,3-0.5 cm, sulle pareti prospicienti dei due vasi e la creazione tra di essi di un’anastomosi latero-laterale. I1 sangue così cortocircuitato provoca rigonfiamento ed a lungo andare una vera e propria arterializzazione delle vene dell’avambraccio; in questo modo un flusso continuo ottimale di 250-30 ml di sangue al minuto può essere ottenuto mediante ripetute successive punture venose, senza l’applicazione di alcuno shunt artificiale permanente.
La metodica seguita da questi autori prevede vari tempi: a) Applicazione di un laccio prossimalmente al gomito al fine di facilitare il rigonfiamento dei vasi. b) Scelta dei punti per la puntura ed iniezione in essi di una piccola quantità di procaina. c) Puntura prossimale direzione prossimale dell’ago ritorno venoso al paziente. d) Spostamento del laccio distalmente alla prima puntura. e) Puntura distale direzione dell’ago verso la mano settore arterioso dal paziente al rene.
Al termine della dialisi gli aghi sono rimossi ed un bendaggio compressivo è applicato su entrambe le sedi di puntura. Ulteriori modificazioni di questo tipo di fistola sono state adottate da Sperling e coll. (1967), i quali anziché effettuare un’anastomosi latero-laterale ne eseguono una termino-terminale i cui vantaggi sarebbero principalmente una più facile tecnica operatoria ed una migliore e più prolungata arterializzazione venosa e da Bartos e coll. (EDTA - Paris 67), i quali hanno proposto l’uso di uno speciale tunnel di fibrina. In questo metodo l’arteria prescelta la cui avventizia viene rimossa per una certa lunghezza viene introdotta nel tunnel di Fibrina e la sua estremità arrovesciata a dito di guanto viene saturata a catgut all’altro capo del tunnel; successivamente la vena viene portata a ricoprire il tunnel stesso e fissata anch’essa mediante catgut. I vantaggi del metodo sono da ricercarsi principalmente nel fatto che l’intima vasale dell’anastomosi non viene sottoposta a traumatismi e che il tunnel di fibrina viene assorbito nel giro di sei mesi, risultandone un’anastomosi composta esclusivamente di tessuto vasale.
I1 flusso sanguigno fornito dai vari tipi di shunt e dalle fistole artero-venose varia tra minimi di circa 150-180 e massimi di 300 cc/minuto, con optimum differenti a seconda del tipo di rene artificiale usato, ma aggirantisi intorno ai 200 cc/minuto. Un interrogativo spontaneo è se, sia gli shunts artificiali permanenti che le fistole sottocutanee, dando luogo ad un corto-circuito arterovenoso possano provocare un aumentato lavoro cardiaco ed essere quindi causa di inconvenienti a breve od a lunga scadenza. Secondo Nickerson e coll. si può avere in detti casi un considerevole aumento del volume cardiaco ed un peggioramento di un eventuale scompenso cardiovascolare, ma secondo altri autori non è stata osservata alcuna variazione del volume cardiaco in seguito ad interruzione sperimentale della fistola arterovenosa.
EPARINIZZAZIONE -
I1 complesso circuito extracorporeo costituito dal rene artificiale e dalle linee arteriosa e venosa di allacciamento al paziente rende necessaria, durante l’effettuazione dell’applicazione emodialitica, 1’eparinizzazione, al fine di impedire la coagulazione del sangue.
L’eparinizzazione si può eseguire in modi diversi: a) Eparinizzazione continua. Si attua mediante infusione attraverso un gocciolatore (linea venosa), od attraverso la linea arteriosa, ed in questo caso necessita l’uso di una pompa per vincerne la pressione sanguigna. b) Eparinizzazione intermittente. Si tratta della metodica più semplice da eseguire e meno costosa. Si tratta di iniettare una certa quantità di eparina (150 mg- 3cc.) attraverso la linea arteriosa all’apertura della dialisi e proseguire poi l’iniezione di eparina ad intervalli regolari e per tutta la durata dell’applicazione, ad esempio 25 mg (1/2 cc.) ogni tre ore. Naturalmente le dosi di eparina da iniettare e la loro frequenza saranno variate a seconda delle circostanze e del paziente sino a giungere alla dose ottimale per impedire senza eccessi la coagulazione nel circuito extracorporeo.
c) Allorché si esegua il trattamento emodialitico in pazienti in cui per particolari condizioni sia controindicato allungare il tempo di coagulazione del sangue e vi sia pericolo di comparsa di emorragie, si ricorre alla tecnica dell’eparinizzazione regionale. Indicazioni a questa tecnica sono quindi da considerarsi le recenti operazioni chirurgiche, l’ematuria, l’ulcera gastrica e duodenale ed ogni tipo di sanguinamento in atto o potenziale. L’eparinizzazione regionale è una metodica più complessa e costosa delle precedenti, perché richiede l’uso di una pompa in grado di fornire un flusso assai basso e di mantenerlo costante per tutta la durata della dialisi. Essa ha il fine di rendere incoagulabile il sangue nel circuito extracorporeo senza che l’organismo del malato risenta dell’effetto della sostanza anticoagulante. Ciò si ottiene infondendo in modo continuo una soluzione di eparina nella linea arteriosa subito distalmente allo shunt e neutralizzandone l’effetto mediante infusione pure continua di una soluzione di solfato di protamina nella livea venosa, prima che il sangue ritorni al paziente. In tal modo è possibile mantenere il tempo di coagulazione del sangue a valori elevati all’interno del dializzato(>20’), mentre nell’organismo esso è di valori intorno ai normali (<10’) ed in ogni caso mai tali da raggiungere livelli di pericolosità.
Per l’effettuazione dell’eparinizzazione regionale vengono utilizzate nella Clinica Medica dell’Universitià di Torino delle pompe rotanti Watson-Marlow che agiscono su tubi di gomma inseriti su due comuni apparati da fleboclisi. Queste fanno capo a due flaconi da 500 cc. di soluzione fisiologica glucosata in cui sono state introdotte opportune dosi rispettivamente di eparina e di solfato di protamina, e cioè 8 cc. di eparina, corrispondenti a 40.000 U.I. nel primo, e 8 fiale (40 cc.) di solfato dì protamina 1% nel secondo. La velocità di infusione dell’eparina e della protamina viene regolato variando la velocità delle pompe e controllata visivamente attraverso due gocciolatori (Figura N° 5); la velocità di iniezione è generalmente di 7-8 gocce al minuto per l’eparina e di 9-10 gocce al minuto per il solfato di protamina.
Figura N° 5 -Dializzatore Kiil e pompe Watson-Marlow per eparinizzazione regionale.
Un inconveniente dell’eparinizzazione regionale è stato osservato recentemente da alcuni autori. Esso consiste in un notevole aumento del tempo di coagulazione del sangue - che può raggiungere i 40-45 minuti - che si verifica talvolta nelle ore successive alla dialisi in cui si è fatto uso dell’eparinizzazione regionale, nonostante le dosi relative dell’eparina e della protamina fossero del tutto corrette. Questo fenomeno, che costituisce un potenziale pericolo per il paziente, è stato definito l’anticoagulation rebound, e raggiunge, secondo Hampers e coll., che l’hanno studiato particolarmente, una frequenza assai più elevata di quanto risulti dalla letteratura attualmente esistente in proposito.
Studi compiuti da questi autori hanno dimostrato come non vi sia in genere una chiara relazione tra l'entità del rebound e la quantità totale di eparina infusa durante la dialisi, e come i tempi di coagulazione registrati in caso di rebound siano usualmente maggiori di quelli osservati in ogni momento nel corso della dialisi.
Questo fenomeno è dovuto ad un ritardato aumento dell’azione eparinica: a) per tardiva reimmissione in circolo di eparina dai linfatici e dall’interstizio, oppure più probabilmente b) per dissociazione del complesso protamina-eparina, risultante in un eccesso relativo di quest’ultima. La possibilità del verificarsi di una tale evenienza sottolinea la necessità di un controllo delle condizioni dei pazienti sottoposti ad emodialisi mediante eparinizzazione regionale, e specialmente del tempo di coagulazione nelle ore successive alla dialisi, che qualora risulti aumentato per il verificarsi del rebound può essere riportato rapidamente alla norma mediante iniezione e.v. di una adeguata dose di solfato di protamina.
Apertura e chiusura della dialisi –
La metodica da noi adottata per procedere all'apertura ed alla chiusura dell'applicazione emodialitica è assai semplice e correntemente eseguita dal personale infermieristico. Essa viene attuata facendo uso di guanti, vestaglie e bavagli sterili, e consta schematicamente delle seguenti operazioni :
per 1’apertura:
a) Disinfezione della cute e dello shunt mediante alcool jodato e mercurocromo.
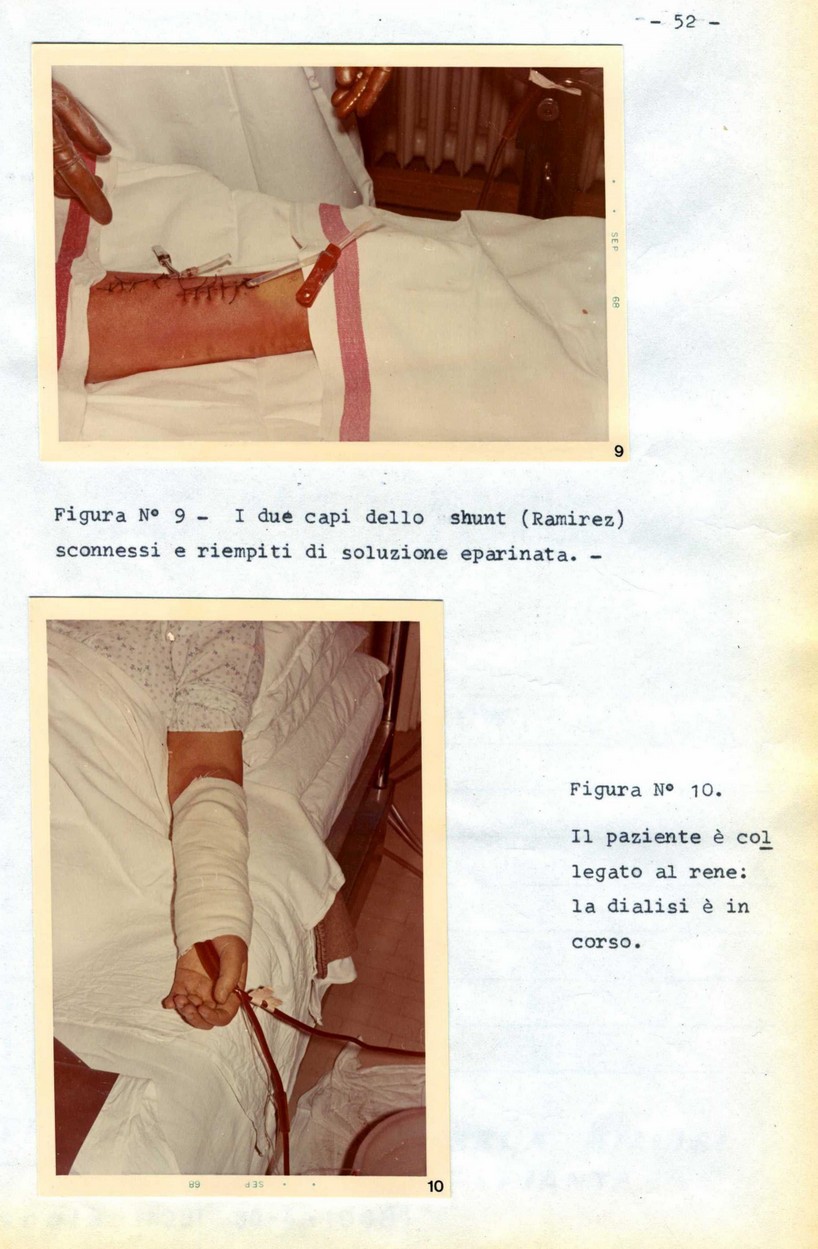
b) Applicazione di pinzette ai due rami dello shunt ed apertura dello stesso (Figure n° 6 e 9) .
c) Eventuale prelievo di sangue (Figura n° 7).
d) Iniezione di 10 cc. di soluzione eparinata nella linea venosa dello shunt (Figura n° 8).
e) Collegamento della linea arteriosa dello shunt al rene artificiale, ripieno di soluzione fisiologica.
f) Penetrazione nel rene di 100cc. di sangue.
g) Collegamento della linea di uscita del rene con la linea venosa dello shunt (Fig. n° 10).
per la chiusura:
a) Applicazione di pinzette e sconnessione del settore arterioso del paziente al rene.
b) Eventuale prelievo di sangue.
c) Iniezione di 100 c.c. di soluzione fisiologica nella linea arteriosa dello shunt.
d) Restituzione al paziente del sangue contenel dializzatore.
e) Interruzione della linea di ritorno del sangue al paziente.
f) verifica delle condizioni del ponte in tee collegamento dei due capi dello shunt tra di loro.
g) Disinfezione della cute e dello shunt a mezzo di alcool jodato e mercurocromo. Bendaggio.
Le Figure n° 6, 7, 8, 9, 10 illustrano alcune fasi delle manualità di apertura dell’emodialisi.

SCELTA DEL PAZIENTE
Un problema di fondamentale importanza è rappresentato dalla scelta dei pazienti da sottoporre al trattamento emodialitico. Innanzitutto dalle statistiche a disposizione è facile dedurre come attualmente solo una percentuale estremamente ridotta dei pazienti che necessiterebbero di un trattamento cronico con il rene artificiale possa venire trattata, e ciò naturalmente aumenta l'importanza di operare una scelta guidata da precisi criteri di opportunità. Facendo alcuni esempi, secondo Shackman nel Regno Unito e nel '6'7 è stato trattato solo il l0% dei potenziali pazienti, mentre altri autori sottolineano come si abbiano ogni anno in media dai 20 ai 30 nuovi malati di insufficienza renale cronica per ogni milione di abitanti e 6000-7000 decessi all'anno per questo motivo nei soli Galles ed Inghilterra. Tutto fa pensare che queste valutazioni, per quanto approssimative, corrispondano alla realtà e siano valide anche per il nostro paese. E' quindi chiaro come, allo stato attuale delle cose, 1'introduzione di un nuovo paziente in un programma caratterizzato, come quello emodialitico periodico, da una ridottissima disponibilità di posti,dalla scadenza indefinita e da numerosi ed improblemi clinici, nonché da una complessità non indifferente, ponga come prima condizione per il suo successo una selezione dei potenziali pazienti.
Una volta riconosciuta 1a necessità di questa scelun nuovo quesito si pone : da chi questa scelta deve venire effettuata? Da medici (un medico od un gruppo di medici), o, come proposto da alcuni autori emesso in pratica presso il centro emodialitico di Seattle, da una apcommissione di laici, visto il rapporto dei medici ? Forse una commissione del genere potrebbe fornire una maggaranzia di imparzialità e distacco, ma è da chiese una commissione di laici sia o meno in grado di valutare adeguatamente nella sua complessità l'aspetto medico e clinico dei problema.
Per quel che riguarda i criteri che debbono guidare la scelta, si può parlare innanzitutto di criteri di ordine medico e quindi di ordine psicologico, eticoed economico. I requisiti generalmente richiesti e quindi indispensabili sono:
a) un'insufficienza renale progressiva non reversibile,
b) assenza di altre malattie gravi che possano interfee compromettere la riuscita del trattamento, ed in particolare assenza di ipertensione maligna o grave e di lunga durata o di una situazione cardiovascolare compromessa,
c) presumibile possibilità di una riabilitazione dei pasino a condizioni di vita soddisfacenti,
d) età del paziente non troppo giovane né troppo avanzata, in media tra i 17 ed i 45-50 anni.
In definitiva questi criteri fondamentali tendono alscelta di un paziente con una malattia renale primaria senza coinvolgimenti o contemporanea compromissione di altri organi ed apparati. A questo proposito è da valutarsi anche 1'evolutività della compromissione della funzione renale, cosa che può essere fatta considerando la creatininemia, il volume della diuresi, l'entità dell'albuminuria ed i valori del filtrato glomerulare (Havilland, Corà, Confortini).
Non minore importanza è da attribuirsi alle condizioni di circolazione delle estremità, poiché pregresse fleprovocate da ripetute punture venose limitano in modo notevole le zone di possibile inserzione degli shunts (Mc Leod).
Vi sono poi criteri di ordine psicologico, che metl'accento sulla necessità di una buona maturità psicologica, sull'equilibrio psichico e la volontà di colpalesata dal paziente. Di conseguenza in numerosi centri emodialitici i potenziali pazienti vengosottoposti prima dell'accettazione ad un'accurata indagine psicologicocon esclusione dei sogpresentanti turbe od instabilità sotto questo punto di vista. Infine non sono trascurabili altri aspetti della questione, come le condizioni sociali ed economidel paziente. autori fanno osservare, con loindubbiamente stringente ma forse eccessivamente rigida, come, essendo di entità notevole per la società la spesa che viene effettuata per aiutare questi pazienti a sopravvivere e soprattutto a raggiungere una riabiliessa debba essere compensata mediante la sceldi pazienti in grado di essere, per la loro condizione sociale, di maggior vantaggio per la società stessa. Ad aggravare ulteriormente questo problema concorre il costo, a tutt'oggi assai elevato dei trattamento e le inadeguate possibilità finanziarie di gran parte dei pazienti. Di conseguenza anche l'aspetto economico fa senla sua influenza: ad esempio Phillips e coll. rifecome nel loro centro emodialitico nel Massachusvenga data priorità ai pazienti di quello stato, poiché lo stato stesso fornisce gli aiuti finanziari necessari al suo funzionamento.
All'opposto, in altri casi, vengono presi in conpuramente i criteri di scelta medici, e sul la base di questi i pazienti vengono accettati come “primo arrivato, primo servito". (Gombos e coll.).
Riassumendo si può dire che il problema della sceldei pazienti per 1'emodialisi rappresenti, specialmente per quel che riguarda i criteri socioe psicologici, un capitolo aperto ed in continua e prevedibimodificazione, viste le continue migliorie e modifidel trattamento ed i sussidi economici che in alcuni stati (USA, Inghilterra), sono devoluti alla creaed al mantenimento di nuovi centri (Phillips).
Riportiamo a titolo di esempio (Tabella N° 6) lo schema delle condizioni che devono guidare la scelta del paziente secondo Havilland (Seattle) :
TABELLA N° 6
1) Individuo stabile, emozionalmente maturo, responsabile.
2) Assenza di ipertensione di lunga data e di complicazioni permanenti.
3) Palese volontà di cooperazione.
4) Età (17-50 anni fisiologici).
5) Deterioramento lento della funzionalità dei rene (creatinina 8-12 mg per 100 ml).
6) Residenza nella zona da sei mesi.
7) Vantaggio per la società.
8) Possibilità finanziarie.
9) Possibilità di riabilitazione.
10) Compatibilità psicologica e psichiatrica.
(Havilland – Seattle - USA)
C A S I S T I C A
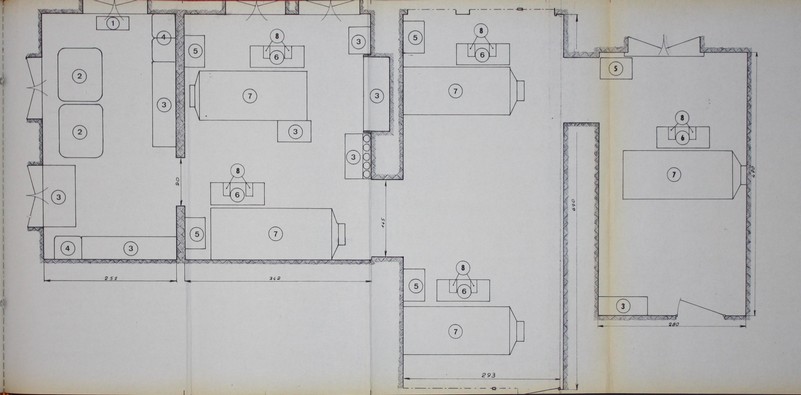
A1 30/6/1968 sono stati trattati nel Centro Emodella Clinica Medica dell'Università di To8 pazienti affetti da insufficienza renale cronica iperazotemica, per un totale di 395 applicazioni, corrispondenti a circa 4400 ore di dialisi ed al trattamento di un singolo paziente per 46 mesi.
I pazienti, 4 di sesso maschile e 4 di sesso femminile, erano di età compresa tra i 24 (minimo) ed i 56 anni (massimo), con un'età media di 38-39 anni.
In 5 di questi pazienti la malattia responsabile dell'insufficienza renale è stata identificata come glomerulonefrite cronica e nei rimanenti rispettivamente come pielonefrite cronica, pielonefrite con calcolosi e pielonefrite con tubercolosi renale.
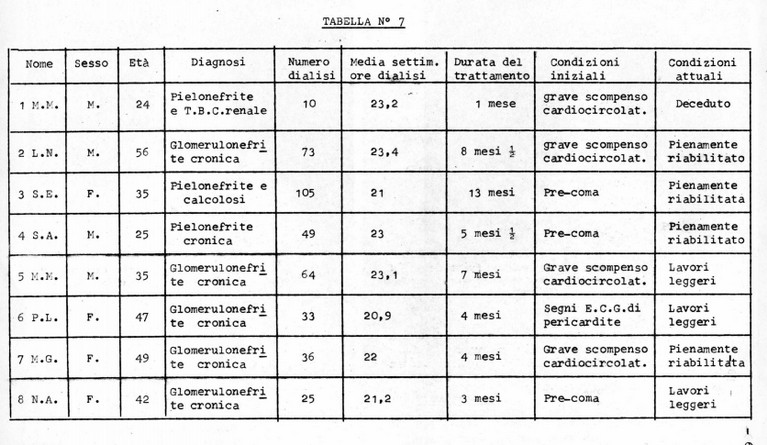
I dati riferiti sono esposti riassuntivamente nella tabella N° 7 .
Al momento del loro ingresso nel programma emodialitico cronico la totalità dei pazienti si trovava in uno stadio uremico che poteva venir considerato come terminale, in quanto ormai refrattario e non ulteriormente controllabile con la consueta terapia medicamentoso-dietetica.
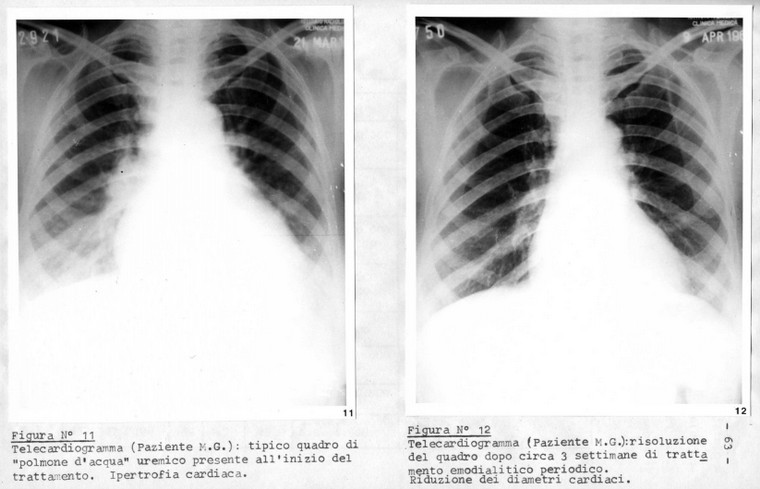
La sintomatologia uremica era rappresentata clinicamente da alito urinoso, edemi, cefalea, ipereccitabilità neuropsichica, vomito, irregolarità del respiro e del polso. I1 telecardiogramma ha rilevato la presenza di un quadro di polmone uremico in tutti i pazienti (Figure n° 11-12), i quali presentavano anche un notevole grado di anemizzazione. Era inoltre presente in 3 casi (3-4-8) uno stato di pre-coma in 4 (1-1-5-7) un grave scompenso cardiocircolatorio, ed in un caso (6) segni elettrocardiografici di pericardite. Nei pazienti S.A. e M.M. (4-5) esami per la ricerca del sangue occulto nelle feci dimostrarono positività alla prova con la benzidina. Indagini radiografiche evidenziarono nel primo caso accentuate note di duodenite con immagine di diverticolo a carico della piccola curvatura duodenale, nel secondo un'immagine di nicchia da lesione ulcerosa nel recesso laterale del bulbo duodenale.
La seguente tabella (N° 3) illustra i valori dell'azoto e della pressione arteriosa all'inizio del trattamento, entrambi di molto superiori alla norma, nonchè i dati di laboratorio relativi alla sodiemia, potassiemia, riserva alcalina, emocromo, quadro proteico.
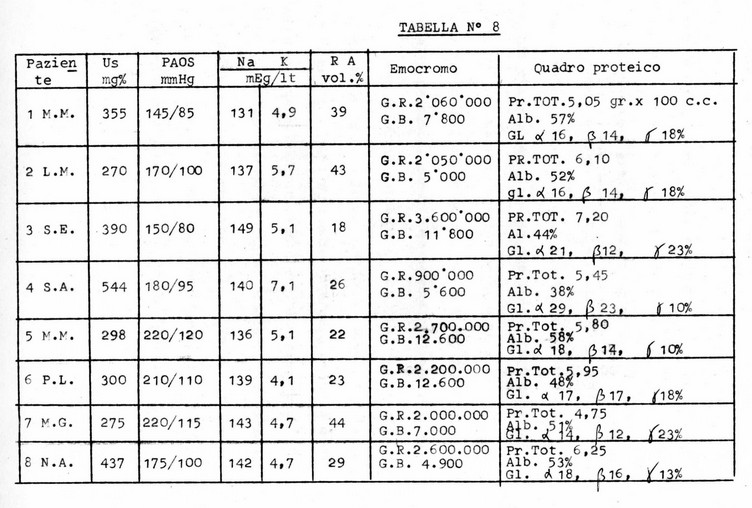
Sei pazienti su otto hanno subito, prima di essere immessi nel programma emodialitico periodico, un ciclo più o meno lungo di dialisi peritoneale. I1 paziente L.N. è stato introdotto nel nostro programma di emodialisi cronica quando era già sottoposto ad un analogo trattamento da circa sei mesi presso un altro centro.
A questi pazienti è stata praticata l'emodialisi mediante rene artificiale Kiil bisettimanalmente con applicazioni ciascuna di circa 12 ore di durata (media settimanale di ore dialisi massima 24 h, minima 20,9 h). In tutti i pazienti il primo periodo è stato caratterizzato dalla presenza, durante la seduta emodialitica, di più o meno spiccati fenomeni di disagio e malessere quali agitazione psicomotoria, cefalea, nausea, vomito, cardiopalmo etc. Particolarmente interessante sotto questo aspetto è un episodio confusionale, con convulsioni di tipo jaksoniano senza perdita di coscienza, intervenuto al paziente S. A. durante una delle prime sedute emodialitiche e verosimilmente attribuibile ad una troppo rapida rimozione dell'azoto ureico dal sangue causata dall'emodialisi, responsabile del passaggio di liquido - per legge osmotica - dal torrente circolatorio al liquido cefalo-rachidiano e conseguente subcerebrale. Si tratta di quella che è stata definita daautori americani "disequilibrium syndrome". Superato questo periodo iniziale si è assistito in tutti i pazienti ad un rapido miglioramento sia sotto l'aspetto clinico che umorale.
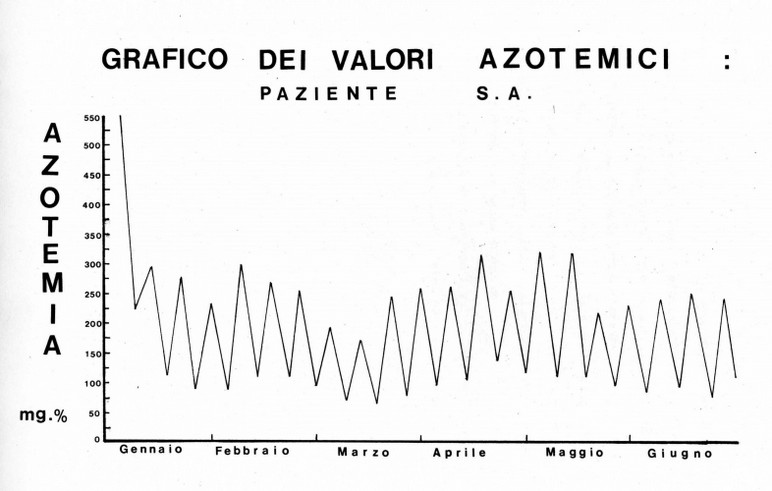
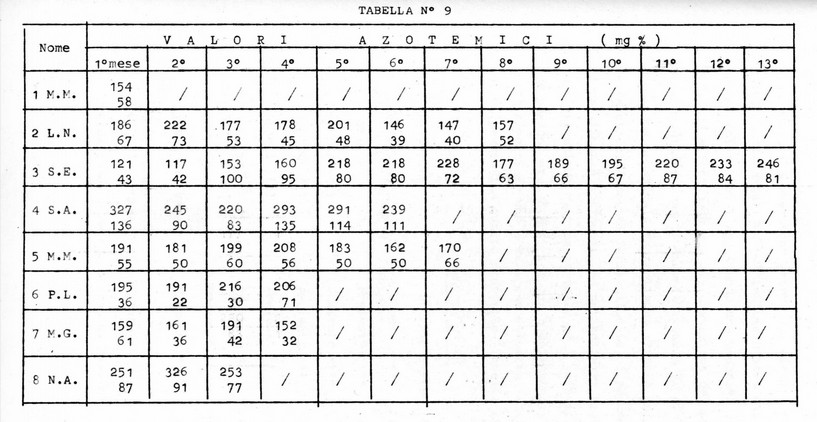
I valori dell'azoto ureico sono notevolmente diminuiti, mantenendosi quelli predialitici generalmente al di sotto dei 250 mg% e quelli post-dialitici al di sotto dei 100 mg%, con differenti livelli a seconda dei diversi pazienti. E' da sottolineare come questi pazienti cronici mostrino di sopportare senza alcun grande disturbo clinico valori azotemici intorno ai 200 mg % ed anche superiori.
La tabella N° 9 espone i valori azotemici medi mensili pre e post-dialitici dei nostri pazienti:
I valori della pressione arteriosa, elevati in tutti i pazienti sono andati normalizzandosi e sono risultati facilmente controllabili applicando una moderata deplezione in sodio ed effettuando una disidratazione dei pazienti durante 1'emodialisi, mantenendo il liquido di dialisi ad una pressione negativa e controllando il peso dei pazienti facendo uso di appositi letti-bilancia. I pazienti sono stati mensilmente sottoposti ad un'inchiesta riguardante la loro situazione clinica generale ed i principali disturbi che possono presentarsi nel corso dell'emodialisi. Qui sotto riportiamo uno schema che dimostra la situazione dei nostri pazienti a questo proposito (Tabella N° 10) :

Non è stato ritenuto opportuno ricorrere per i nostri pazienti a periodiche sistematiche trasfusioni di sangue, ma si è ricorso ad esse solamente quando, per svariate cause (ad esempio coagulazioni delle piastre del rene artificiale, rotture delle membrane di cellophane), si fosse verificata una perdita di sangue, o quando i valori dell'ematocrito scendessero a troppo basso livello: la tabella n° 11 mostra il bilancio ematico dei nostri pazienti nei mesi da Gennaio a Giugno 1968, ed i corrispondenti valori medi pre e postdialitici dell'ematocrito
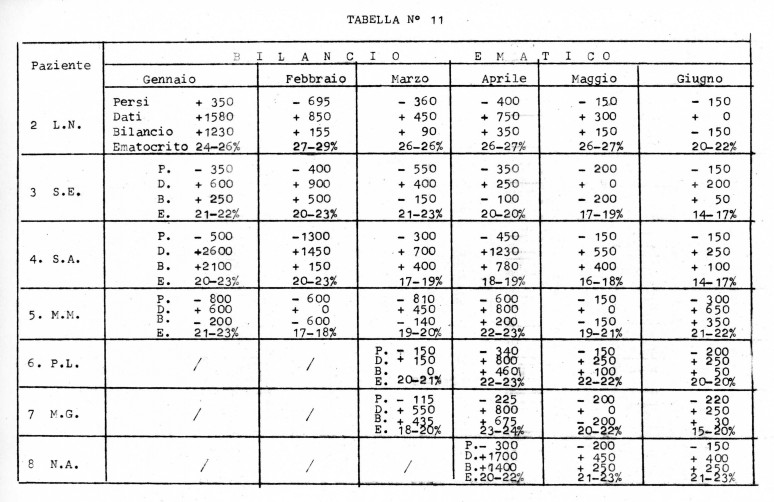
Di questo gruppo di 8 pazienti sottoposti ad emodialisi periodica 7 sono attualmente sopravviventi : la totalità di questi ha raggiunto un ottimo grado di riabilitazione, e precisamente 4 sono pienamente riabilitati ed in grado di svolgere normalmente la loro abituale attività, mentre 3 sono in grado di svolgere lavori leggeri, come è mostrato dalla tabella n° 12 :
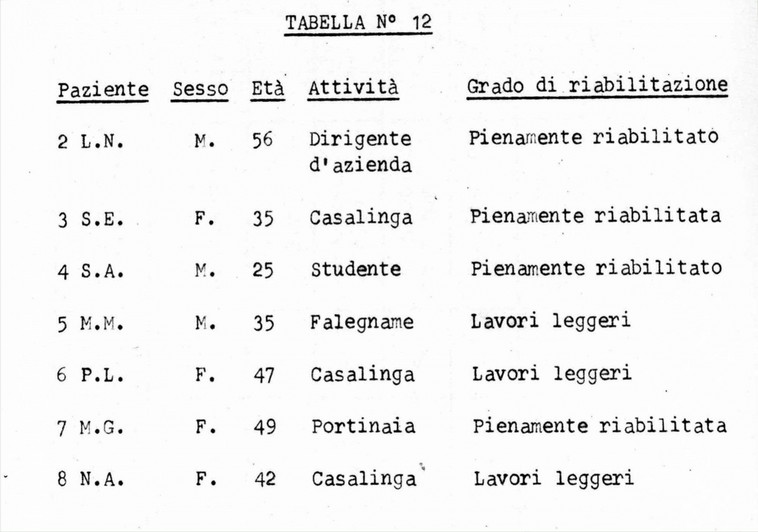
I1 paziente 1 M.M. è deceduto dopo un mese di trattamento e 10 applicazioni di rene artificiale in seguito ad un episodio di polisierosite tubercolare.
La tabella N° 13 riporta la situazione dei nostri pazienti per quanto riguarda i valori azotemici, la pressione arteriosa, elettroliti, riserva alcalina, emocromo e quadro proteico al 31 giugno 1968, a fina dialisi :
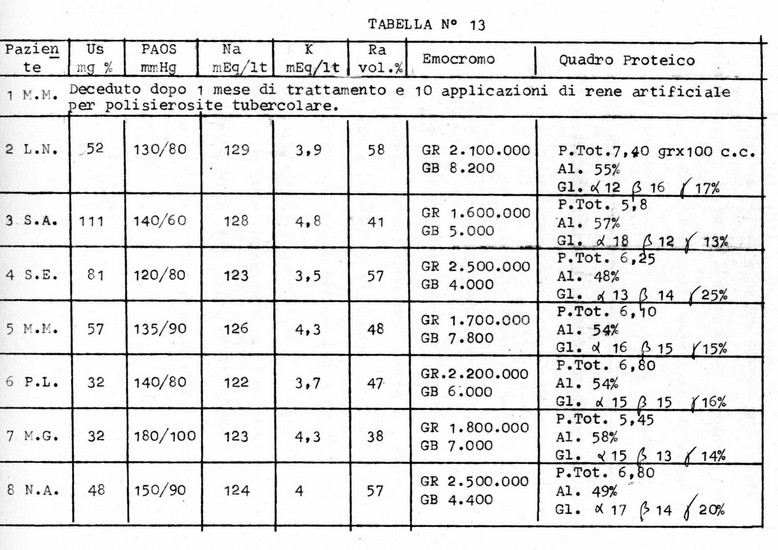
Come si può osservare i valori azotemici, degli elettroliti e della riserva alcalina si sono normalizzati. Pure normalizzati sono i valori pressori, con una sola eccezione. Non altrettanto soddisfacenti sono i valori dell'emocromo. La depressione del numero dei globuli rossi è solo in parte da attribuire alla cronica perdita di sangue cui sono soggetti questi pazienti, per gli abituali prelievi di laboratorio e per la quantità per quanto esigua tuttavia non trascurabile di sangue che non può venir restituita al paziente e rimane nel dializzatore al termine dell'emodialisi. Non è da sottovalutare poi, il probabile intervento di fattori mielotossici ostacolanti l'eritropoiesi, nonché di un'aumentata emolisi, da causa plasmatica extraglobulare.
I pazienti non accusano attualmente una evidente sintomatologia imputabile ad uremia. Sono tuttavia presenti un grado più o meno spiccato di astenia in tutti i pazienti, prurito persistente in due casi, cefalea in quattro, ma esclusivamente durante la dialisi, ed in tre pazienti rari episodi saltuari di nausea e vomito, anche questi solamente nel corso dell'applicazione emodialitica.
L'appetito è buono in 4, discreto in altrettanti.
In tre pazienti sono presenti parestesie, specialmente agli arti inferiori; in altri tre pazienti sono riscontrabili nei primi due saltuari crampi agli arti inferiori, nel terzo diminuzione del visus. In un solo paziente erano presenti segni cutanei di deficit della coagulazione, ma essi sono regrediti da quando si è introdotto l'uso dell'eparinizzazione regionale, e da allora anche l'abbassamento visivo di un paziente è notevolmente migliorato.
Per quanto riguarda la terapia seguita, tre pazienti seguono con ottimo esito terapia anticoagulante con sintron. Gli incidenti (coagulazione) a carico degli shunt sono scomparsi da quando detta terapia è stata istituita. Tutti seguono terapia con polivitaminici. Nessun'altra terapia è praticata. La dieta è libera, ma deve contenere almeno 2000 calorie e circa 50-60 grammi di proteine.
Nel periodo di circa un anno è stato eseguito un totale di 395 applicazioni bisettimanali di rene artificiale per un totale di 4400 ore di dialisi. E’ stato utilizzato il rene artificiale tipo Kiil a due compartimenti dializzanti ed in un numero limitato di casi il Kiil a tre compartimenti. Le dialisi sono state eseguite facendo uso della metodica dell'eparinizzazione regionale e con singolo passaggio del liquido di dialisi senza ricircolazione ad una temperatura di 37-38 gradi centigradi.
Ogni applicazione ha avuto una durata media genedi 11 ore e 1/2 circa, mentre la media settimanadi ore dialisi ha variato da un minimo di 20,9 ore per la paziente P.L. ad un massimo di 24 ore settimanali per la paziente S.E.
Nel periodo contemplato dalla presente casistica si sono verificate 7 coagulazioni delle piastre del rene artificiale e 18 rotture delle membrane di cellophane, che hanno provocato l'interruzione delle rispettive applicazioni; in più è da registrare un imprecisato numero di coagulazioni parziali delle piastre, che non sono state causa di interruzione della seduta emodialitica.
E' inoltre da segnalare un caso nel quale due dialisi vennero temporaneamente interrotte a causa di mancanza della corrente elettrica della rete stradale con conseguente arresto della pompa del liquido di dialisi. I dati relativi sono riportati nella seguente tabella riassuntiva (N° 14) .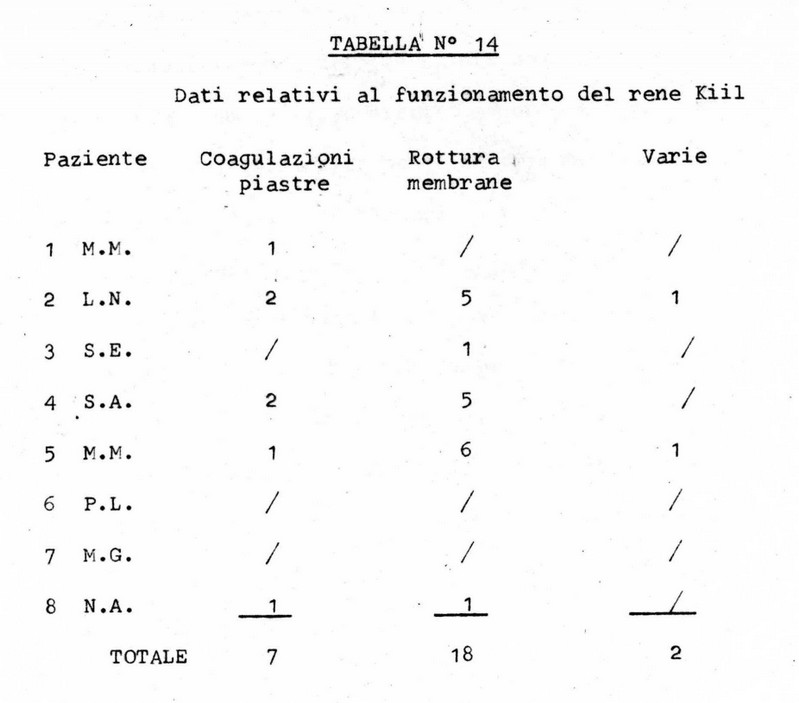
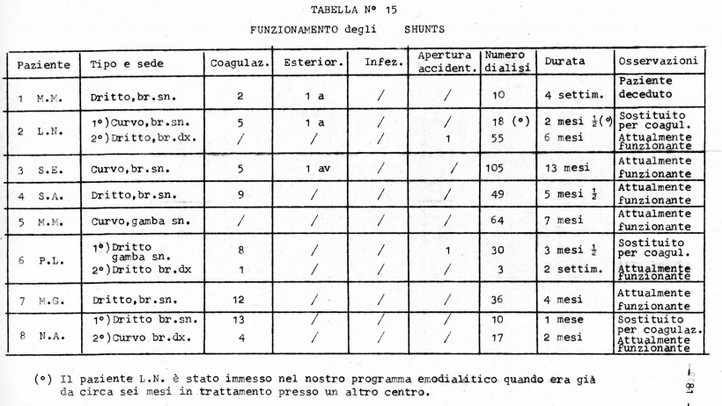
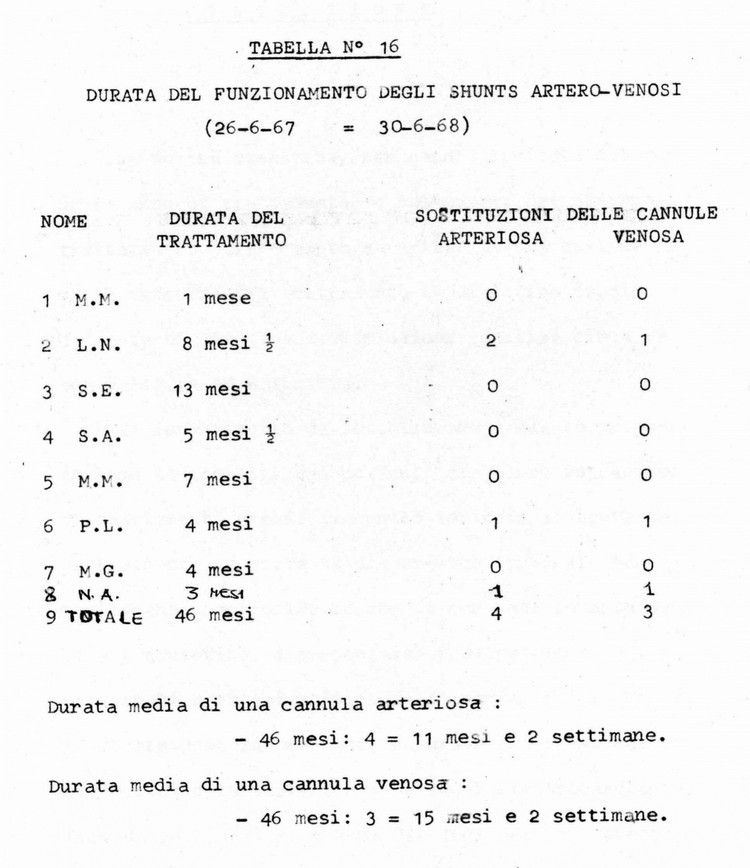
Per quel che riguarda i by-pass antero-venosi 3 shunts su 8 hanno dovuto essere sostituiti nel periodo preso in considerazione (37%); in tutti e tre i casi la causa della sostituzione è stata la coagulazione del sangue all'interno dello shunt stesso. E' stato quindi fatto uso in totale di 11 shunts dei quali 4 del tipo curvo di Scribner e 7 del tipo diritto di Ramirez. Gli shunts per cui non si è resa necessaria la sostituzione (5), e quelli usati per la sostituzione nei tre casi rimanenti sono a tutt'oggi perfettamente funzionanti (Tabelle N° 15 e 16). Per la sostituzione dei tre shunts coagulati ne sono stati usati due di tipo diritto ed uno di tipo curvo.
I1 luogo prescelto per l'inserzione degli shunts è stato in 6 casi l'avambraccio sinistro, in 3 casi l'avambraccio destro ed in 2 casi la. gamba sinistra.
Nel periodo compreso dalla presente casistica si sono verificate in totale 59 coagulazioni negli shunts, di cui alcune a ritmo subentrante nei casi delle pazienti P.L., M.G. e N.A.. Tutti questi episodi di coagulazione (tranne 3 che hanno resa necessaria la sostituzione dello shunt) sono stati risolti facendo uso di mezzi meccanici od enzimatici (streptochinasi, 1 caso). Sono inoltre da segnalare 2 casi di esteriorizzazione della linea arteriosa stessa, ed un terzo caso di iniziale esteriorizzazione di entrambi i settori arterioso e venoso con relativo intervento di riposizione.
In due casi si è verificata 1'apertura accidentale della linea arteriosa dello shunt nel corso dell'emodialisi; in entrambi i casi si è verificata un'emorragia di circa 100 cc. di sangue senza conseguenze per il paziente. Non si sono mai verificati episodi di infezione degli shunts.
I dati relativi agli shunts artero-venosi sono riportati schematicamente nelle Tabelle N° 15 e 16.
D I S C U S S I 0 N E
La nostra casistica, per quanto limitata nel tempo (1 anno di trattamento) e nel numero dei pazienti trattati (8), offre ampio materiale di discussione circa la metodica del trattamento emodialitico cronico e consente di giungere a conclusioni positive circa la sua validità ed efficacia.
E' innanzitutto da sottolineare a questo proposito come la totalità dei pazienti che hanno intrapreso il trattamento presso il centro torinese si trovasse inizialmente in grave stadio uremico terminale non ulteriormente controllabile con la consueta terapia medica e dietetica, e presentasse inoltre alcuni dei principali problemi clinici dell'uremia, quali uno stato di pre-coma in tre casi, un grave scompenso cardiocircolatorio in quattro casi e segni elettrocardiografici di pericardite in uno. Nel 100% dei casi questo stadio critico è stato superato in seguito al trattamento emodialitico.
I criteri da noi adottati come guida alla scelta dei pazienti da introdurre nel programma emodialitico sono stati i più ampi possibili. Ad esempio, per ciò che riguarda l'età, non tutti i nostri pazienti rientrano nei limiti consigliati dall'esperienza di altri centri (età abitualmente ritenuta massima 45anni), ma i risultati del trattamento non si differenziano in alcun modo da quelli ottenuti negli altri pazienti più giovani. Confortati da questi risultati riteniamo di non includere un'età tra i 50 ed i 60 anni tra le rigide controindicazioni al trattamento emodialitico periodico.
Parallelamente all'età altri elementi che avrebbero potuto precludere ai nostri pazienti la possibilità d'ingresso in un programma emodialitico cronico qualora ci si fosse rigidamente attenuti ai criteri di Havilland (Seattle), NcLeod, Phillips, Shaldon, Schreiner etc., sono lo stato di pre-coma o di scompenso cardiocircolatorio presente in tutti i nostri pazienti all'inizio del trattamento.
E' chiaro come nessuno dei nostri pazienti fosse in possesso di tutte le caratteristiche richieste, e ciò nonostante il trattamento è stato coronato da successo nella totalità dei casi. L'unico decesso registrato nella nostra casistica è da attribuirsi infatti a cause esterne sopravvenute (polisierosite tubercolare) e non all'uremia, e si é verificato dopo 1 mese e 10 applicazioni dall'inizio del trattamento emodialitico, quando già il quadro idroelettrolitico ed i valori azotemici e pressori erano in via di normalizzazione con conseguente scomparsa della sintomatologia uremica.
Criteri così, estensivi quali quelli da noi adottati nella scelta dei pazienti sono anche giustificati dal fatto che in alcuni dei nostri pazienti (S.E. - M.G.) si è iniziato il trattamento confidando in una riacutizzazione del processo cronico, evento che non si è però verificato.
Traducendo in cifre i nostri dati, si vede come 1'unico decesso da noi registrato nel corso del trattamento emodialitico cronico rappresenti una percentuale di mortalità del 12,5%, valore assai basso se confrontato con la percentuale di mortalità registrata in tutta Europa secondo i dati forniti dall'E.D.T.A. al congresso di Dublino del Giugno 1968 (Tabella N° 17), che, pur diminuendo ogni anno progressivamente, ha tuttavia raggiunto nel 1968 il valore del 31% dei pazienti.

Per ciò che riguarda le cause di morte durante il trattamento emodialitico le statistiche europee riportano (Tabella N° 18) al primo posto l'insufficienza cardiaca (ed è suggestivo pensare che forse l'aumentato lavoro cardiaco di questi pazienti portatori di grosse fistole artero-venose artificiali non sia estraneo nel mantenere lo scompenso cardiaco al primo posto di questa statistica), al secondo, con una percentuale d'incidenza di molto inferiore, le infezioni, al terzo incidenti vascolari cerebrali, ed infine edema cerebrale, cachessia, infarto miocardico, errori tecnici ed epatite virale.

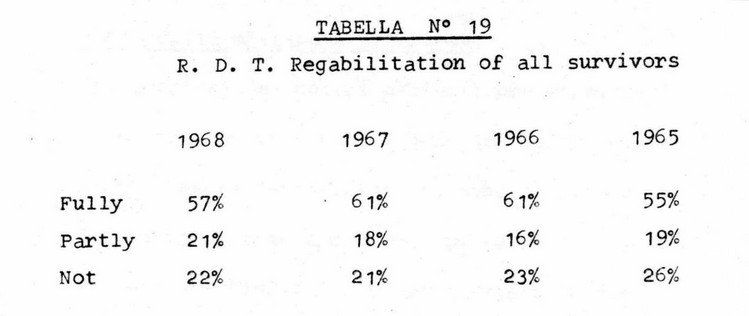
Tuttavia lo scopo del trattamento emodialitico cronico non è una semplice sopravvivenza fine a se stessa, ma una sopravvivenza in condizioni tali da consentire una riabilitazione del paziente, e quindi un suo reinserimento attivo nella propria famiglia e la ripresa dell'attività lavorativa. Questo obbiettivo è stato raggiunto in tutti i nostri pazienti. Come si è dettagliatamente riferito in precedenza nella casistica, quattro pazienti su sette sono da considerarsi pienamente riabilitati, in quanto hanno ripreso con successo l'attività lavorativa, mentre altri tre sono riabilitati parzialmente in quanto sono in gradi svolgere lavori leggeri. Ciò corrisponde ad una percentuale del 57,1% di riabilitazioni complete e del 42,9% di parziali, mentre nessun nostro paziente è classificabile come non riabilitato. Questi dati appaiono incoraggianti qualora confrontati con la percentuale di riabilitazione raggiunta in tutta Europa nel 1968 (TaN° 19), che comprende il 57% di pienamente riabilitati, il 21% di riabilitati parzialmente e ben il 22°/ di pazienti non riabilitati
L'ottima riabilitazione di questi pazienti, la scomparsa completa dei sintomi imputabili all'uremia cronica in seguito al semplice trattamento emodialitico costituiscono dei dati di partenza per ricerche di estremo interesse, e pongono in discussione quanto della sintomatologia uremica sia reversibile. Le lesioni anatomiche sono certamente irreversibili, ma certamente si può affermare in definitiva che la totalità della sintomatologia clinica dell'uremia può essere corretta mediante l'uso periodico del rene artificiale.
Altri problemi di estrema importanza che si presentano nel corso del trattamento dialitico cronico sono quelli concernenti il controllo della pressione arteriosa, dell'emocromo e del bilancio azotato, nonché alcune interessanti complicazioni del trattamento stesso.
Controllo della pressione arteriosa.
La totalità dei nostri pazienti presentava, all'inizio del trattamento, valori pressori notevolmente elevati. Attualmente detti valori si sono normalizzati in tutti i pazienti tranne uno, nel quale tuttavia, pur rimanendo elevati (180/ 100) , si sono sensibilmente ridotti rispetto agli originali (220/115).
Pensiamo quindi di poter affermare che è possibile ottenere, nel corso del trattamento periodico col rene artificiale, un buon controllo della pressione arteriosa. I mezzi da noi adottati a tal fine sono i seguenti
1) controllo costante del peso del paziente mediante riduzione dell'apporto idrico e salino durante il periodo interdialitico. L'aumento di peso nel periodo interdialitico non deve generalmente superare i 2 Kg.
2) Ultrafiltrazione. All'inizio della seduta emodialitica, considerati i valori pressori, le condizioni cliniche e l'eccesso di peso rispetto al peso ideale per quel depaziente, viene programmato il peso che si desidera il paziente raggiunga al termine della dialisi. Creando una pressione negativa nel compartimento del liquido dializzante si ottiene un'ultrafiltrazione utilissima nel caso di pazienti iperidratati, edematosi, ipertesi o presentanti il tipico quadro del "polmone d'acqua" uremico. Mediante ultrafiltrazione è possibile far perdere ad un paziente sino a 3-4 Kg. di peso nel corso di una seduta di 12 ore.
3) Deplezione sodica nel liquido di dialisi. Diminuendo moderatamente il tasso di sodio nel liquido di dialisi è notevolmente facilitato il controllo della pressione arteriosa dei pazienti dializzati. I1 bagno di dialisi da noi attualmente utilizzato contiene sodio nella percentuale di 136,85 mEq/lt, valore assai vicino a quello normale plasmatico.
L'associazione di queste tre differenti metodiche ha così risolto uno dei più pressanti problemi clinici dei pazienti in dialisi periodica; gli unici effetti coi laterali negativi di questa metodica sono infatti rappresentati dalla possibilità di comparsa di episodi di ipotensione ortostatica al termine della dialisi, o di cranipi muscolari da iposodiemia, inconvenienti a cui è possibile ovviare con facilità.
Controllo della crasi ematica.
L'anemia è un sintomo costante dell'uremia cronica. Essa è generalmente considerata come un'anemia iporigerativa ed attribuita a depressione midollare conseguente alla tossicosi uremica e da iperemolisi da causa explasmatica. In corso di trattamento con rene artificiale altri fattori anemizzanti entrano in gioco, quali la cronica perdita di sangue determinata dai frequenti prelievi di laboratorio o conseguente a quelle sia pur piccole, tuttavia non trascurabili quantità di sangue che non possono venir restituite al paziente e rimangono nell'apparecchio al termine della seduta emodialitica.
A questi fattori è probabile si debba aggiungere un certo grado di emolisi che il sangue subirebbe durante il passaggio nell'apparecchio, entrando in contatto con le varie parti che lo compongono. La concomitanza di questi vari fattori fa sì che questi pazienti presentino - come è concordemente rilevato da tutti gli autori - una notevole tendenza all'anemizzazione, controllabile mediante ripetute trasfusioni. In effetti tutti i nostri pazienti presentano valori ematologici notevolmente ridotti, alcuni più bassi che non all'inizio del trattamento. Come già è stato ricordato in preceza non è stato ritenuto opportuno ricorrere ad un programma sistematico e prestabilito di trasfusioni, ma si è seguito il criterio di ridurre le stesse alla quantità minima, in considerazione della non remota possibilità dell'istaurarsi in questi pazienti politrasfusi di situazioni allergiche di intolleranza. Si è quindi ricorso a trasfusioni solo in caso si dovesse reintegrare il patrimonio sanguigno depauperato da emorragie (rotture del cellophane, coagulazioni nel rene artificiale o qualora i valori dell'ematologico e dell'ematocrito scendessero a troppo basso livello.
Un tentativo di verifica dell'ipotesi, avanzata da alcuni autori, che 1'eccessivo numero di trasfusioni fosse anch'esso responsabile dell'anemia di questi pazienti, attraverso un fenomeno di inibizione midollare, ha dato esito negativo; in cinque periodi di un mese quattro nostri pazienti non hanno ricevuto trasfusioni; in tutti i casi i valori dell'ematocrito si sono conseguentemente ridotti.
Equilibrio azotato ed idroelettrolitico.
La regolazione dell'equilibrio azotato dei pazienti in emodialisi periodica coinvolge numerosi aspetti del trattamento ed in modo particolare la frequenza e la durata delle dialisi ed il tipo di alimentazione.
La nostra esperienza porta a considerare ottimale una dialisi bisettimanale della durata di 10ore ciascuna. In alcune occasioni infatti in cui, per particolari situazioni contingenti - coagulazione del sangue nel rene artificiale o nello shunt, con conseguente otturazione del medesimo - si è dovuto ridurre la durata dell'applicazione o addirittura saltarla, i valori azotemici predialitici successivi si sono subito riportati a livelli notevolmente elevati. In pazienti di mole corporea superiore al normale o di corporatura atletica è senz'altro utile nel controllo dei valori azotemici l'uso del rene Kiil a tre compartimenti dializzanti anziché a due, il quale possiede il 50% in più di superficie dializzante.
I1 tipo di alimentazione rappresenta un problema strettamente connesso al precedente, poiché è stato dimostrato (Giordano) che con una dieta assai ipoproteica è possibile ridurre la durata e la frequenza delle dialisi. E' inoltre opportuna, ai fini di un buon controllo dei valori pressori e del bilancio idroelettrolitico, una restrizione idrica e salina. Allo stato attuale delle conoscenze ci sembra tuttavia opportuno l'apporto di una quota calorica e proteica ottimale, aggirantesi su valori di minima di 50-60 grammi di proteine e 2000 calorie giornaliere. Un regime di questo genere sembra influire inoltre positivamente anche su di uno degli aspetti collaterali negativi del trattamento emodialitico cronico, e cioè sulle neuropatie periferiche. Pare infatti (Della Rosa) che questo tipo di complicanze possa recedere in seguito ad un aumento della somministrazione proteica.
Complicazioni del trattamento emodialitico.
Aumentando progressivamente il numero dei pazienti sottoposti ad emodialisi periodica ed accrescendosi 1'esperienza clinica in proposito, sono assurte a notevole importanza clinica alcune interessanti complicazioni del trattamento emodialitico, e precisamente la neuropatia periferica, la "pseudogotta", le calcificazioni metastatiche e 1'iperparatiroidismo secondario.
a) Neuropatia periferica. Questa sindrome, identificata per primo da Osler (1892), ha recentemente acquistato notevole importanza in relazione all'emodialisi periodica, in quanto può costituire un ostacolo di notevole importanza alla piena riabilitazione dei pazienti dializzati.
La sintomatologia di questa interessante forma è rappresentata da alterazioni sensitive quali dolori, bruciori, iperestesie od intorpidimento cutanei alle estremità distali degli arti, specialmente gli inferiori, e da alterazioni motorie quali riduzione dei riflessi, astenia e debolezza muscolare. In quattro dei nostri pazienti sono presenti alterazioni di questo tipo e precisamente
Paziente L.N. : formicolii ai polpastrelli della mano destra.
Paziente S.E. : senso di "scossa elettrica” alle caviglie durante la deambulazione.
Paziente M.M. : formicolii e dolorabilità diffusa al le braccia ed alle gambe.
Paziente S.A. : formicolii e senso di intorpidimento diffuso agli arti inferiori, asteniamuscolare.
Solamente in quest'ultimo paziente, tuttavia, i sintomi hanno raggiunto un'entità notevole; è stato di conseguenza praticato un esame elettromiografico che ha evidenziato uno stato di sofferenza neurogenica, denunziato da un'attività elettrica da contrazione volontaria alquanto ridotta e da un aumento dei tempi di conduzione motoria del nervo tibiale posteriore lungo la gamba.
La causa della comparsa di questa complicazione nel corso del trattamento emodialitico periodico è tuttora sconosciuta. Non si tratta di una complicazione su base vitaminica carenziale, in quanto essa non è influenzata da una massiva somministrazione di vitamine (Konotey-Ahulu, Shaldon). Numerosi autori sono invece propensi a ritenere che un tempestivo e precoce inizio del trattamento emodialitico nei pazienti uremici cronici possa prevenire la comparsa di questa forma, la quale sarebbe anche influenzata positivamente da un adeguato apporto calorico e proteico, e soprattutto da un aumento nella frequenza e nella durata della dialisi (McLeod). Si tratterebbe quindi in definitiva non di una complicazione del trattamento emodialitico, ma bensì di una manifestazione che comparirebbe in pazienti sottodializzati e direttamente conseguente a dialisi inadeguata.
b) Pseudogotta, calcificazioni metastatiche ed iperparatiroidismo secondario.
Nei pazienti sottoposti ad emodialisi cronica è stata descritta da alcuni autori (Caner) una sindrome pseudogottosa rappresentata clinicamente da attacchi del tutto simili a quelli gottosi, con formazione di veri e propri tofi, ed attribuita da alcuni (Naher) a depositi di fosfato di calcio. Benché un simile quadro sintomatologico non sia mai stato riscontrato nei nostri pazienti, occorre sottolineare come la totalità degli stessi presenti abitualmente dei valori uricemici predialitici notevolmente elevati, sino a 10-12 mg %, mentre i valori postdialitici sono di molto inferiori e pressoché vicini alla norma (intorno ai 5-6 mg%) . I1 problema è tutt'ora insoluto e le pubblicazioni in proposito scarse e contrastanti nelle loro interpretazioni dei fenomeno; detto problema è tuttavia certamente meritevole di più approfondito studio.
Un altro aspetto notevolmente importante e poco noto delle complicazioni del trattamento emodialitico è quello che riguarda il metabolismo calcico di questi pazienti. Numerosi autori segnalano il manifestarsi di una sintomatologia artritica e la formazione di focolai di calcificazione metastatica in sede articolare ed in vari organi, quali i reni ed il cuore, o, all'opposto, la comparsa di demineralizzazioni ossee nei pazienti in emodialisi cronica. All'autopsia inoltre di alcuni di questi pazienti, deceduti dopo periodi più o meno lunghi di trattamento, gli stessi autori hanno riscontrato la presenza di una spiccata iperplasia delle ghiandole paratiroidi (Maher).
E' evidente come la notevole diversità dei reperti faccia intravedere la complessità dei problemi coinvolti in quello più generale del metabolismo calcico di questi pazienti. Nei nostri pazienti tuttavia radiografie delle ossa mascellari e delle estremità degli arti non hanno messo in evidenza altro che generiche note artrosiche e qualche modesto focolaio di demineralizzazione ossea.
A proposito di questa serie di complicazioni del trattamento emodialitico riportiamo un interessante prospetto riassuntivo (Tabella N° 20), fornito dall'E.D.T.A. al congresso di Dublino del 1968, il quale testimonia, su di una base di 2633 pazienti, l'incidenza notevolmente elevata delle stesse nei vari centri emodialitici europei negli ultimi tre anni. Da questi dati si dedurrebbe l'influenza positiva esercitata dal trattamento emodialitico nei confronti della neuropatia e della pseudogotta, mentre esso non avrebbe apprezzabile effetto sulle calcificazioni metastatiche ed agirebbe addirittura negativamente nei confronti dell'iperparatiroidismo secondario.
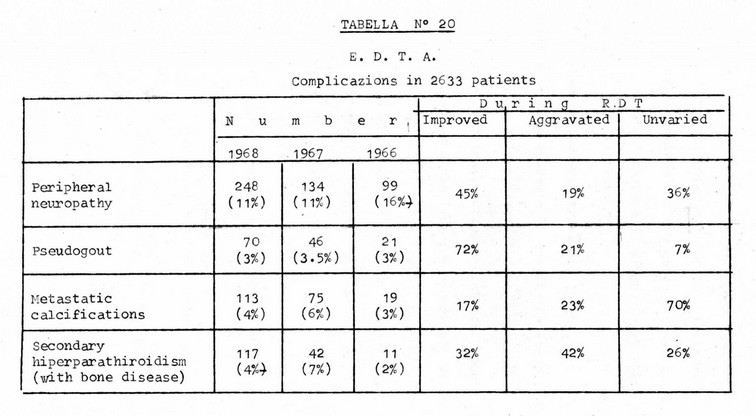
A queste complicazioni, data la peculiarità del trattamento emodialitico cronico, che si vale di un complesso circuito extracorporeo sottoposto a numerose manipolazioni, nonché richiede con una certa frequenza 1'effettuazione di ripetute trasfusioni, si deve aggiungere l'epatite virale.
Numerosi autori (Friedman, Jones), riportano casi di vere e proprie epidemie di epatite da siero, con numerosi casi letali, sviluppatesi in centri renali, colpendo non solamente i pazienti sottoposti al trattamento col rene artificiale, ma anche medici e membri del personale. In Europa e nel 1968 (E.D.T.A. 1968), una statistica condotta su 45 centri mette in evidenza ben 177 casi di epatite, di cui 107 tra i pazienti, con 7 morti, e 70 casi tra il personale, con nessun decesso; detto numero di casi è percentualmente superiore a quello dei casi registrati negli anni precedenti, in una statistica su 19 centri (Tabella n° 21) :

Le cause di un simile fenomeno risiedono certamente nella notevole facilità di infezione cui detti pazienti ed il personale addetto ad essi sono sottoposti per via dell'elevato numero di trasfusioni e di manipolazioni del sangue degli stessi pazienti e di donatori che il trattamento richiede. Una relazione tra trasfusioni di sangue ed epatite è possibile scorgere dalla tabella N°22 (E.D.T.A.), la quale riporta la percentuale di presenza di manifestazioni epatitiche o meno rispettivamente in centri A, ove vengono eseguite trasfusioni solo in casi di emergenza, centri che rappresentano il 16% di quelli con epatite ed il 20% di quelli senza epatite; e centri B+C, ove vengono praticate trasfusioni regolarmente od allorché l'anemia si fa marcata, i quali rappresentano 1'80% dei centri senza e l'84% dei centri con epatite virale.

Nel nostro centro tutti i pazienti sottoposti a dialisi periodica presentano sporadicamente valori delle transaminasi sieriche più o meno alterati (peraltro in un solo caso superiori a 100) , ma in nessuno si è mai clinicamente evidenziata epatite. Nell'estate 1968 un allievo interno che aveva frequentato il centro nella primavera precedente è stato colpito da epatite virale; è tuttavia difficile, essendo il caso isolato, stabilire o meno una relazione tra le due cose.
In ogni caso nel centro emodialitico torinese vengono abitualmente adottate rigorose precauzioni al fine di ridurre al minimo i rischi di contaminazione per i pazienti e per il personale sanitario; tra queste possiamo ricordare l'uso di maschere, vestaglie e guanti sterili durante le manipolazioni di apertura e chiusura degli shunts, nonché nel corso del complesso di operazioni riguardanti lo smontaggio, la pulizia e la preparazione dei reni artificiali.
Discussione sugli aspetti tecnici del trattamento.
Le maggiori difficoltà, per quel che riguarda gli aspetti tecnici del trattamento emodialitico, sono staregistrate nella manutenzione e funzionamento degli shunts artero-venosi. Come già precedentemente riferito nella casistica, nel periodo preso in considerazione si è verificato un elevato numero di complicazioni, la più frequente delle quali è stata la coagulazione (59 episodi). Cinquantasei di questi episodi sono stati risolti facendo uso di mezzi meccanici od enzimaticí (in un caso streptochinasi); in tre casi invece i tentativi di disostruzione non sono stati coronati da successo e si è dovuto procedere alla sostituzione dello shunt.
I dati a nostra disposizione non ci permettono di tracciare un paragone tra lo shunt curvo di Quinton e quello diritto di Ramirez, in quanto entrambi i tipi di shunt hanno presentato episodi di coagulazione in pressoché eguale percentuale, tenendo in debito conto come sia stato fatto uso dei primo in soli 4 casi e del secondo in 7.
Le cause responsabili degli episodi di coagulaziosono a nostro parere da ricercarsi principalmente nell'ipotensione arteriosa o nella compressione esercitata sullo shunt dall'esterno : nella maggior parte dei casi infatti la coagulazione si è verificata in coincidenza di transitori abbassamenti pressori, o durante la notte, circostanza nella quale all'ipotensione fisiologica può essersi sommata occasionalmente, nel diminuire il flusso sanguigno attraverso lo shunt, la compressione del corpo del paziente sullo stesso.
In altri casi (pazienti P.L., N.G., N.A.) le coagulazioni si sono verificate a ritmo subentrante, a poche ore di distanza l'una dall'altra; i motivi di questo fenomeno on sono del tutto chiari, ma almeno in due casi esami flebografici hanno permesso di ricondurli rispettivamente, nel primo, alla presenza di un piccolo coagulo venoso occludente l'estremità del tip dello shunt (Figure N° 15 e 16), e nel secondo ad una particolare condizione anatomica presente nella zona d'inserzione a carico della vena incannulata, la quale pochi centimetri prossimalmente all'estremità del tip si divideva in alcune collaterali (Figura N° 14) .
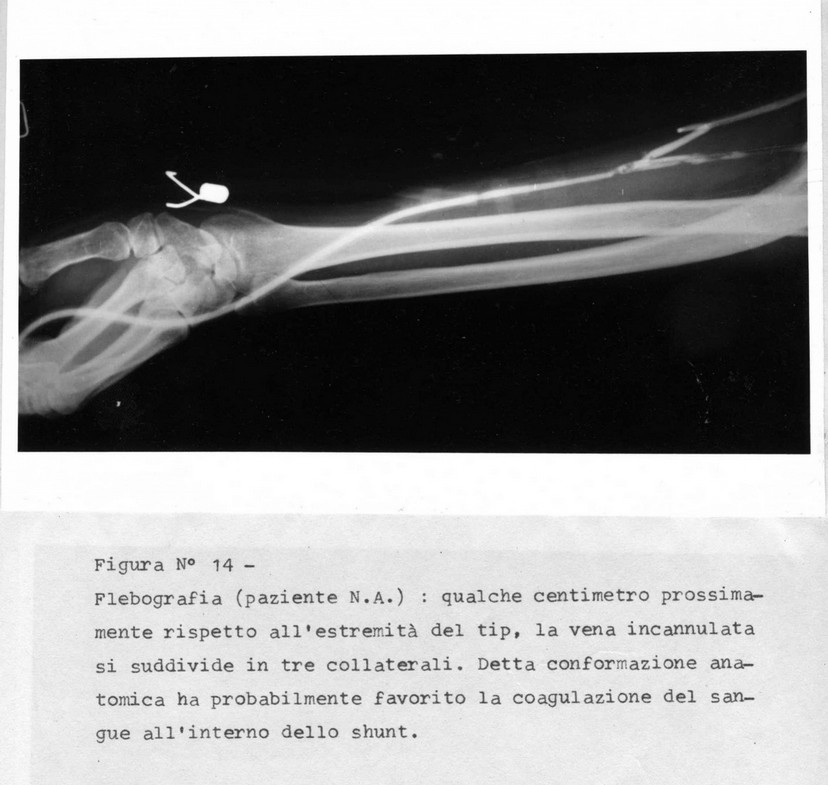
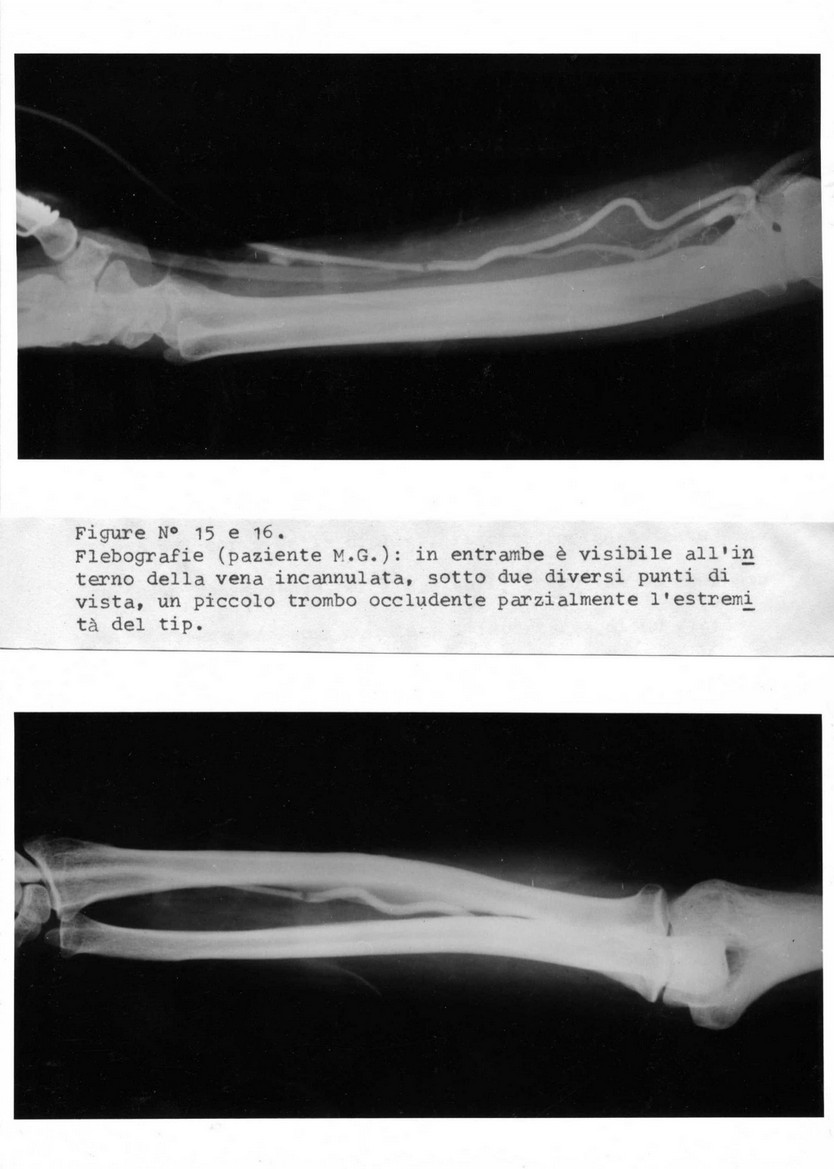
In tre pazienti in cui è stata istituita una terapia anticoagulante con sintrom non si è più verificata alcuna ostruzione degli shunts.
La durata media di una cannula arteriosa è stata di 11 mesi e due settimane, mentre quella di una cannula venosa è stata di 15 mesi e due settimane. Questa differenza è da attribuirsi al fatto che in un caso si è proceduto alla sostituzione della sola linea arteriosa, esteriorizzatasi per erosione della cute soprastante.
I due casi di apertura accidentale della linea arteriosa nel corso della dialisi, risolti fortunatamente senza gravi conseguenze per i pazienti, sottolineano come non potrà essere mai sopravalutata 1' importanza di un vigile controllo dei pazienti stessi nel corso della dialisi, specialmente allorché, durante 1e prime applicazioni, è facile il manifestarsi di alterazioni psichiche quali irrequietezza, eccitabilità, insofferenza, nonché di nausea, vomito e cefalea.
Infine il fatto che non si siano mai verificati episodi di infezione degli shunts, mentre esistono nella letteratura numerose segnalazioni a proposito di infezioni capaci di scatenare setticemie gravissime e talvolta mortali (Stille), o difficilmente domate dagli antibiotici, conforta la nostra opinione della necessità di un'accurata asepsi da parte del personale in tutte quelle operazioni che richiedono manipolazioni degli shunts artero-venosi e del circuito extracorporeo.
Per quel che riguarda il rene artificiale, gli inconvenienti più frequentemente registrati sono stati la rottura delle membrane di cellophane e la coagulazione del sangue all'interno dell'apparecchio. II fatto che le rotture delle membrane si siano verificate in assoluta maggioranza all'inizio dell'applicazione emodialitica ci suggerisce la necessità di una delicata ed attenta manipolazione delle stesse durante la loro sterilizzazione ed il montaggio dell'apparecchio; circa la coagulazione è necessario sottolineare l'opportunità dell’uso di reni con piastre in plexiglass, le quali, essendo trasparenti, permettono di riconoscere a colpo d'occhio questo fenomeno non appena esso inizia a verificarsi, e consentono quindi di apportare nel più breve tempo possibile le modifiche necessarie alle reciproche proporzioni tra eparina e solfato di protamina.
C 0 N C L U S I 0 N E
Secondo la nostra esperienza l'emodialisi cronica (12 ore bisettimanali) ha dimostrato di essere una metodica valida a permettere la sopravvivenza e la riabilitazione di pazienti in grave stato uremico terminale, quando la terapia medica e dietetica si siano rivelate inefficaci. La normalizzazione della situazione idroelettrolitica, dei valori azotemici e pressori ottenibile dall'emodialisi periodica permette il superamento delle condizioni più critiche dell'uremia cronica ed il successivo reinserimento di questi pazienti nel consorzio sociale e, nella maggior parte dei casi, la ripresa della precedente attività lavorativa.
In un futuro assai prossimo inoltre, l'introduzione della metodica della dialisi notturna e della dialisi a domicilio del paziente, già attuate in alcuni centri inglesi ed americani, migliorerà ulteriormente le prospetti ve sotto questi punti di vista.
Attualmente le maggiori difficoltà alla diffusione ed estensione di tale trattamento sono quelle di natura economica, dato il costo notevole dell'apparecchiatura e della metodica e le disponibilità generalmente inadeguate dei pazienti. Un tale stato di cose è tuttavia in via di evoluzione e negli ultimi anni si è assistito ad un notevole diffondersi in tutto il mondo del trattamento emodialitico periodico dell'uremia cronica, mentre alcuni autori segnalano le facilitazioni finanziarie che in alcune nazioni (U.S.A., Inghilterra) vengono devolute ai centri impegnati in un tale programma. I dati dell'E.D.T.A. relativi all'incremento dei centri emodialitici in Europa e negli ultimi 4 anni (Tabella N° 23) mostrano come siano attualmente esistenti in Europa 114 centri, contro i 43 del 1965, con un incremento di più del 150%., per un totale dl 1281 pazienti attualmente in trattamento.
La mortalità dei pazienti in emodialisi è passata dal 41% nel 1965 al 31% nel 1968, mentre sono in aumento pure i pazienti che, dopo un periodo più o meno lungo di emodialisi vengono indirizzati al trapianto.
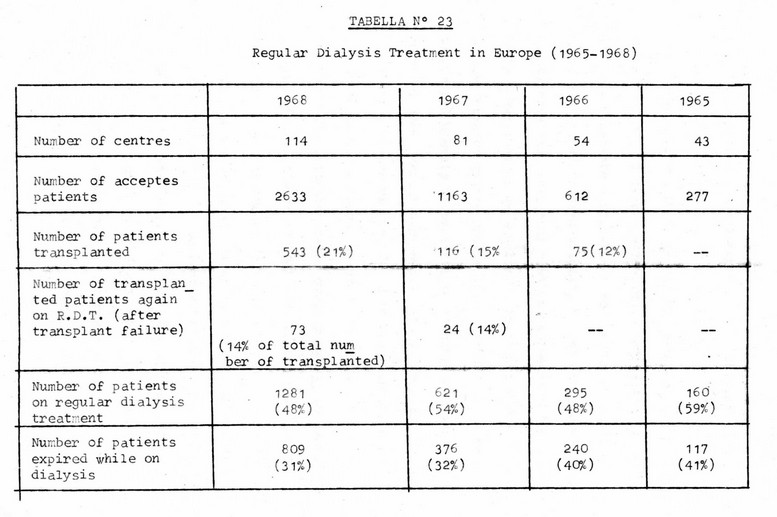
La sempre maggiore esperienza ed i successi conseguiti dal trapianto renale sollevano infine il quesito di quale sia la futura funzione del trattamento emodialitico periodico. Potrà essere esso fine a se stesso, sviluppandosi organicamente attraverso numerosi centri guidati e coordinati da un "centro pilota", o esso sopravviverà con una diversa finalità, cioè come una metodica indispensabile in previsione di un successivo trapianto ? E' possibile che entrambe queste possibilità coesistano. Un numero sempre più elevato di pazienti sottoposti ad emodialisi cronica, verrà certamente indirizzato al trapianto renale, visti i sempre più rapidi ed incoraggianti progressi compiuti in questo campo; ma nel caso di pazienti cui il trapianto sia controindicato, quali pazienti anziani, con lesioni arteriosclerotiche diffuse, oppure nel caso di mancanza di un donatore vivente dell'organo da trapiantare o di non disponibilità di un rene idoneo di cadavere, l’emodialisi periodica con rene artificiale rappresenteà ancora una metodica insostituibile. E' così paradossalmente possibile che, in un domani non molto lontano, l'emodialisi periodica trovi il suo maggior campo d'applicazione in quelle situazioni in cui è oggigiorno controindicata.
R I A S S U N T 0
Viene studiata 1'efficacia del trattamento emodialitico periodico nel consentire la sopravvivenza e la riabilitazione dei pazienti affetti da insufficienza renale cronica iperazotemica in grave stadio uremico terminale, non ulteriormente controllabile con la consueta terapia medicamentosa-dietetica. Viene riportata a tal scopo l'esperienza compiuta nella Clinica Medica dell'Università di Torino eseguendo il trattamento emodialitico periodico per un anno su 8 pazienti, per un totale di 395 applicazioni di rene artificiale Kiil, corrispondenti a circa 4400 ore di emodialisi ed al trattamento di un singolo paziente per 46 mesi.
Detto trattamento ha portato, nella totalità dei casi, al superamento delle critiche condizioni iniziali ed alla normalizzazione dei valori azotemici, pressori, e della situazione idroelettrolitica, con conseguente scomparsa della sintomatologia uremica. In 7 casi su 8 è inoltre stata ottenuta la riabilitazione del paziente (totale in 4 casi, parziale in 3) con piena ripresa dell'attività lavorativa. L'unico decesso registrato è da attribuirsi a cause esterne sopravvenute (polisierosite tubercolare), e non all'uremia, e si è verificato quando già il quadro idroelettrolitico ed i valori azotemici e pressori si erano normalizzati in seguito al trattamento.
I dati ottenuti da detta casistica vengono discussi e confrontati con quelli relativi alla situazione europea del trattamento emodialitico periodico, forniti dal 1'European Dialysis and Transplant Association al congresso di Dublino del Giugno 1968, nei confronti dei quali dimostrano una minor percentuale di mortalità, una maggior percentuale di riabilitazioni ed una più bassa incidenza di complicanze.
Vengono inoltre illustrati e discussi gli aspetti tecnici del trattamento e confrontati criticamente i vari tipi di reni artificiali e di shunts artero-venosi attualmente esistenti.
Lo studio compiuto permette di giungere a conclusioni positive circa la validità e l'efficacia del trattamento emodialitico periodico dell'insufficienza renale cronica, e di valutarne le prospettive future in rapporto al trapianto renale.
E ' possibile concludere che l’emodialisi periodica, oggi fine a se stessa, rappresenterà fra non molto da una parte una metodica indispensabile in funzione ed in previsione di un successivo trapianto, dall'altra una certezza di sopravvivenza e di riabilitazione per i pazienti cui il trapianto sia controindicato.
B I B L I 0 G R A F I A
Abella R., Blondeel N., Roguska J., Walker C., Simon N., and Del Greco F.
"Periodic Dialysis in Terminal Uremia"
J.A.M.A. 199: 362-8, 6 Feb. 1967.
Ackman C., Handa S., Morrin P., and Bruce A.
"An artificial kidney system suitable £or multiple simultaneous dialysis"
Canad. Med. Ass. J. 96: 528-30, 4 Mar. 1967.
Anderson A., Kolff W.
"Artificial kidney in the treatment of uremia associated with acute glomerulonephritis (With a note on regional heparinization)"
Ann. Intern. Med. 51: 476-87, 1959.
Brandon J., Nakamoto S., Rosenbaum J., Franklin M. and Kolff W.
"Prolongation of survival by periodic prolonged hemodialysis in patients with chronic renal failure"
Amer. J. Med. 33: 335.44, Oct. 1962.
Brescia M., Cimino J., Appel K., and Hurwich B.
"Chronic hemodialysis using venipuncture and a surgically created arteriovenous fistula"
New Eng. J. Med. 275: 1089-92, 17 Nov. 1966.
Bunn H., Kurt H., Rubin A., and Glenn D.
"Limited success of intermittent dialysis in chronic renal disease"
J.A.M.A. 188: 785-90, 1 June 1964
Caner J. et al.
"Recurrent acute (gouty?) arthritis in C.R.F. treated with periodic hemodialysis"
Amer. J. Med., 36: 571-82, Apr. 1964.
Captain J., Captain R., Captain T., and major P.E. Teschan
"Efficient heparin assay for monitoring regional heparinization and hemodialysis"
New Eng. J. Med. 262: 654-7, 1960.
Clark P., Chir M., Parsons F.
"Routine use of the Scribner shunt for haemodialysis"
Brit. Med. J. 5497: 1200-2, 14 May 1966
Corà D., Dalla Rosa C., Galanti C., Ancona G., Bruschi E., Confortini P.
"La nostra esperienza nel trattamento delle nefropatie croniche con emodialisi periodiche"
Min. Med. 56: 4263-5, 5 Dic. 1965
Confortini P., Galanti G., Ancona G., Bruschi E., Dalla Rosa C., Corà D.
"Recenti progressi nelladella emodialisi periodica"
Min. Med. 56: 42635 Dic. 1965.
Confortini P., Galanti G., Ancona G., Bruschi E., Dalla Rosa C., Corà D.
"I1 trattamento periodico con rene artificiale delle nefropatie croniche"
Min. Med. 94: 4053-78, 24 Nov. 1965.
Curtis J., Evans D., De Wardener H.
"Disposable arterial and venous sets with connectors £or use with the modified twoKiil kidney"
L ancet 2: 783-4, 8 Oct. 1966.
Evans D., Curtis J., De Wardener H., Storey J., Jennings P.
"Prototype maintenance haemodialysis unit"
Lancet 1: 1012-3, 8 May 1965.
European dialysis and Transplant Association - Parigi 1967, Atti del congresso.
European Dialysis and Transplant Association - Dublino 1968, Atti del congresso.
Freeman R., Maher J ., and Schreiner G.
"Hemodialysis £or chronic renal failure. 1. Technical considerations"
Ann. Intern. Med. 62: 519-34, Mar. 1965
Friedman E., Thomson G.
"Hepatitis complicating chronic haemodialysis"
Lancet 2: 675-8, 24 Sept. 1966.
Galanti G. e coll.
"La nostra esperienza nel trattamento dell'uremia cronica con emodialisi ripetute".
Min. Nefrol. 1: 171-3, Apr.-Giu.1965.
Goldsmith H., Edwards E., Moorehead P., and Wright F.
"Difficulties encountered in intermittent dialysis £or chronic renal failure"
Brit. J. Urol. 38: 625-34, Dec. 1966.
Gombos E., Lee T., Harton M., and Cummings J.
"One year's experience with an intermittent dialysis program"
Ann. Intern. Med. 61: 462-9, Sept. 1964.
Hampers C., Blaufox M., and Merril J.
"Anticoagulation rebound after hemodialysis"
New Eng. J. Med. 275: 776-8, 6 Oct. 1966.
Hansons R., Lindholm T., Lindqui st B., Low B., and Stig-Bertil Nilsson
"Autotransfusion at repeated treatrrents vith the artificial kidney"
Acta Med. Scand. 177: 377-83, Mar. 1965.
Hardenburg H. Jr. et al.
"Extracorporeal hemodialysis in a 350-bed community hospital"
J. Urol. 96: 978-84, Dec. 1966.
Haviland J.
"Chronic hemodialysis: problerrts encountered in a community artificial kidney center"
Morthwest Med. 65: 633-8, Aug. 1966.
Hayes C., Ruby L., and Roscoe R. Robinson
"Long-term intermittent hemodialysis"
J.A.M.A. 195: 1089-94, 28 Mar. 1966.
Heidland A., Kltltsch K., Scheitza E., Pippig L., and Sperling M.
"Klinische Erfahrungen mit der subkutanen arteriovenosen fistel in der Hamodialyse-Behandlung"
Deutsch. Med. Weehr. 92: 427-9, 10 Mar. 1967.
Helliott R. et al.
"Heparin level in haemodialysis"
Lancet 2: 553, 1961.
Hoffler D., Opitz A., Schaefer K.
"Die effektivitgt der Hamodialyse mit der Travenol-niere"
Deutsch. Med. Wachr. 92: 199-204, 3 Feb. 1967.
Jean G., Praga G., Brancaccio D., Della Grazia M., Pisani E.
"Alterazioni della coagulazione in rapporto alla dialisi extracorporea"
Atti Acc. Med. Lomb. 20: 91-95, Apr.-Giu.1965.
Jones P., Glodsmith H., Wright F., Roberts C., Watson D.
"Viral hepatitis a staff hazard in dialysis units"
Lancet 1: 835-40, 15 Apr. 1967.
Keon W., Mangel R., and M. Kaye.
"Three years' experience with bypass cannulae for chronic hemodialysis"
Canad. Med. Ass. J. 96: 524-7, 4 Mar. 1967.
Kolff W.J.
"Medicai History. First Clinical experience with the artificial kidney•'
Ann. Intern. Med. 62: 608-19, Mar. 1965.
Konotey-Ahalu F., Baillod R., Comty C., Heron J., Shaldon S., Thomas P.
"Effect of periodic dialysis in the peripheral neurophaty of end-stage renai failure"
Brit. Med. J. 2 1212-15, 20 Nov. 1965.
Maher J., Freeman R., and Schreiner G.
"Hemodialysis for chronic renai failure. 2. Biochemical and clinical aspects"
Ann. Intern. Med. 62 535-50, Mar. 1965.
Maher J., Lapierre L., Schreiner G., Geiger M., and F.B. Westervelt
"Regional heparinization for hemodialysis"
New Eng. J. Med. 268: 451-6, 1963.
McLeod L., Mandin H., Davidman M., Ulan R., and Lakey W.
"Intermittent hemodialysis in terminal chronic renal failure"
Canad. Med. Ass. J. 94: 318-27, 12 Feb. 1966.
Murray J .
"Transplantation and hemodialysis. 1. The recipient's response to renal transplantation"
J.A.M.A. 198: 307, 17 Oct. 1966.
Nabarro J.
"Who best to make the choise?"
Brit. Med. J. 1:622-4, 11 Mar. 1967.
Parsons F.
"A true doctor's di lemma"
Brit. Med. J. 1: 622-4, 11 Mar. 1967.
Phillips H.
"Hemodialisys center"l
New Engi. J. Med. 276: 1208, 25 May 1967.
Rae A., Pomeroy J., Rosen S., Silva H., and Shaldon S.
"Early attempts at rehabilitation of terminal uremic patients by periodic haemodialysis"
Brit. J. Urol. 37: 325-30, Jun. 1965.
Schreiner G., Maher J.
"Hemodialysis £or chronic renal failure. 3. Medical, moral and ethical, and socio-economic problems"
Ann. Inter. Med. 62: 551-7, Mar. 1965
Schupak E., and J. P. Merril
"Experience with long-term intermittent hemodialysis"
Ann. Intern. Med. 62: 509-18, Mar. 1965.
Scribner B.
"Haemodialysis in the treatment of chronic uremia"
Brit. J. Urol. 38: 607-8, Dec. 1966.
Shackman R.
"Surgeon's point of view"
Brit. Med. J. 1: 622-4, 11 Mar. 1967
Shaldon S., Oakley J.:
"Experience with regular haemodialysis in the home"
Brit. J. Urol. 38: 616-20, Dec. 1966.
Shea E. Borgdan D., Freeman R., and Schreiner G.
"Hemodialysis £or chronic renal failure. 4. Psycological considerations"
Ann. Intern. Med. 62: 558-63, Mar. 1965.
Shimizu A. Kaye N:., and B.J. Innes
"Chronic hemodialysis for terminal renal failure"
Canad. Med. Ass. J. 94: 311-7, 12 Feb. 1966.
Stewart J., and Neale F.
"Dialysis: a comparison of the efficiency of peritoneal dialysis with the artificial kidney".
Med. J. Aust. 2: 210-4, 30 Jul. 1966.
Stewart J., and Le Quesne D.
"The employment of dialysis in general hospitals and in artificial kidney unite"
Med. J. Aust. 1: 262-3, 11 Feb. 1967.
Stille W., Brass H., Hach W., Renner D., Heintz R.
"Shunt-sepsis"
Deutsch. Med. Wschr. 92: 476-72, 17 Mar. 1967.
Swinney J.
"Regular dialysis treatment in Europe and the British isles, 1966”
Brit. J. Urol. 38; 609-12, Dec. 1966.
Tsaltas T.
"Transplantation and haemodialysis; 2. Long-term intermittent hemodialysis and the recipiente”
J. A. M. A. 198 307 , 17 Oct. 1966 .
Yoffa D., and M.C. Vernon
"Arterio-venous cannula £or repeated haemodialysis"
Med. J. Aust. 2: 648-51, 1 Oct. 1966.
Warren W., and D.J. Vincent
"Delayed clinical response to hemodialysis in a patient with uremia".
J. A. M. A. 196: 186-7, 11 Apr. 1966.
Waterhouse K., Friedman E., McDonald H., and C.E. Thomson
"Intermittent hemodialysis for chronic renal failure"
J. Urol. 97: 426-31, mar. 1967.
Wilson M.
"Doctor's duty to his patient”
Brit. Med. J. 1: 622-4, 11 Mar. 1967.
Si ringrazia per la collaborazione tecnica l'ing. M. De Biasio
